同源康医药再次递表港交所:预计2024年继续亏损,核心产品TY-9591进入关键临床试验阶段
格隆汇7月30日丨根据港交所最新消息,7月29日,浙江同源康医药股份有限公司("同源康医药")递交港交所主板上市申请,独家保荐人为中信证券。此前,公司于1月26日已向港交所递交过上市申请。

初步招股书显示,公司是一家临床阶段的生物制药公司,致力于发现、收购、开发差异化靶向治疗并对其进行商业化,以满足癌症治疗中亟待满足的医疗需求。自2017年成立以来,公司已建立由11款候选药物组成的管线,包括核心产品TY-9591、六款临床阶段产品及四款临床前阶段产品。目前正在中国进行TY-9591单药治疗的关键II期临床试验,将其用于表皮生长因子受体("EGFR")突变非小细胞肺癌("NSCLC")脑转移的一线治疗,以及正在中国进行TY-9591单药治疗的注册性III期临床试验,将其用于EGFRL858R突变的局部晚期(IIIb或IV期)或转移性NSCLC的一线治疗。
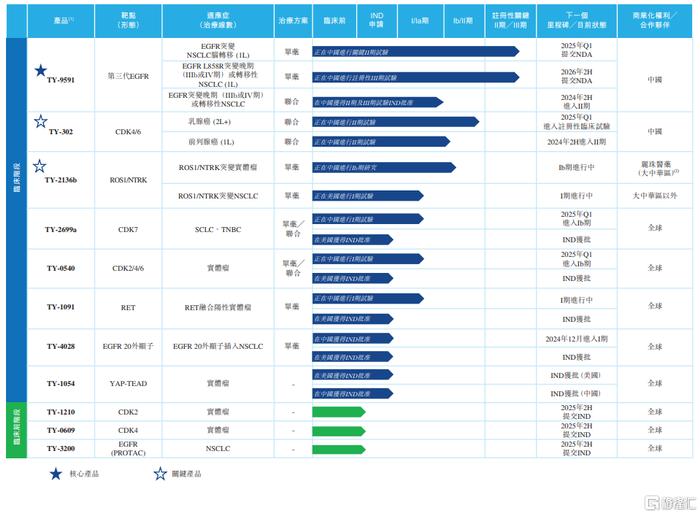
根据弗若斯特沙利文的资料,TY-9591为全球唯一正在进行头对头注册性临床试验以直接比较其与奥西替尼疗效的EGFR-TKI。为充分挖掘TY-9591的潜力,公司亦于2024年3月就进行TY-9591联合培美曲塞及顺铂或卡铂一线治疗EGFR突变晚期或转移性NSCLC的II期及III期临床试验作出申请并已获得IND批准,预计于2024年下半年开始II期试验。
随着公司的核心产品TY-9591进入关键临床试验阶段,公司正在浙江省湖州建设符合cGMP的内部生产设施,预计将于2025年底前开始商业规模生产。公司亦计划通过内部努力并且与外部合作伙伴合作来建立销售及营销能力以确保公司在中国成功商业化该产品。
研发方面,公司持续投入资源,为长期发展铺路,公司于2022年、2023年及截至2024年3月31日止三个月的研发成本分别为人民币2.298亿元、人民币2.493亿元及人民币6470万元。截至2024年3月31日,公司的研发团队有102名成员,其中约60%拥有相关领域的硕士或博士学位。截至最后实际可行日期,公司持有50项已授权专利,包括在中国的16项已授权专利、在美国的一项已授权专利、在其他司法权区的33项已授权专利,以及136项专利申请,包括在中国的43项专利申请、在美国的14项专利申请、在其他司法权区的64项专利申请及PCT项下的15项专利申请。
财务方面,公司的年内亏损由2022年的人民币3.118亿元增加至2023年的人民币3.832亿元,主要是由于(i)毛利减少人民币2000万元。公司的期内亏损由截至2023年3月31日止三个月的人民币8320万元增加至截至2024年3月31日止三个月的人民币1.078亿元。
公司表示,预计截至2024年12月31日止年度仍将随着研发活动的继续推进持续产生净亏损。
此次IPO募资资金将用于公司核心产品(即TY-9591)的研究、开发及商业化;用于公司其他候选产品的研发,包括TY-302、TY-2136b、TY-1091、TY-4028、TY-2699a及TY-0540用于潜在的战略收购、投资、许可或合作机会;及用于营运资金及其他一般公司用途。
