Cell Research | 吴乔课题组发现甘露糖抑制焦亡缓解化疗副作用的新机制
转自:生物谷
细胞焦亡是近年来发现的一种在细胞膜上打孔引起的可调控的细胞死亡形式。目前证实具有执行细胞焦亡功能的蛋白有Gasdermin家族蛋白,包括GSDMA、GSDMB、GSDMC、GSDMD和GSDME。虽然大量研究清楚地阐述了该家族蛋白执行细胞焦亡的机制,但这些蛋白被负调控的机制目前还不清楚。早在2019年,EmadS.Alnemri课题组的研究发现了GSDME蛋白能被磷酸化,磷酸化的GSDMEN端则丧失执行细胞焦亡的能力,然而具体的上游调控机制未阐明。此外,Gasdermin家族蛋白在不同组织间的表达也存在着显著的差异。
邵峰教授课题组以及其他课题组的研究都发现,GSDME在肠道和肾脏中显著高表达,而在大部分肿瘤细胞中则呈现低表达;特别是在化疗过程中,化疗药物引起了组织细胞发生GSDME介导的细胞焦亡,从而诱发严重的毒副作用,由此加重化疗患者的痛苦以及影响治疗的进程。因此,深入解析负调控GSDME蛋白介导的细胞焦亡机制,可能对减轻化疗药物的毒副作用具有一定的临床意义。
2023年7月17日,CellResearch在线发表了吴乔教授团队的最新研究成果:MannoseantagonizesGSDME-mediatedpyroptosisthroughAMPKactivatedbymetaboliteGlcNAc-6P。该研究发现,临床药物甘露糖激活的AMPK可以磷酸化GSDME由此抑制细胞焦亡。在此基础上,课题组把甘露糖引入临床化疗过程,发现甘露糖可以作为辅助药物减轻化疗引起的毒副作用。前期,吴乔课题组已在CellResearch(2018,28(12):1171-1185)报道了铁剂促进临床药物诱导GSDME引起细胞焦亡,从而抑制肿瘤的正调控机制。而这一新的工作则在前期工作的基础上,进一步解析了AMPK负调控GSDME的新途径,并将甘露糖很好地应用于减轻化疗药物引起毒副作用的过程中,阐明了一种老药新用的新颖范式。

甘露糖(Mannose)是葡萄糖的类似物。一旦进入细胞,甘露糖能够通过己糖胺生物合成途径(HBP)提高代谢物GlcNAc-6P含量,促进GlcNAc-6P结合到AMPK,进而有利于LKB1的结合以激活AMPK。活化的AMPK随后在Thr6位点磷酸化GSDME,导致caspase-3不能结合并剪切GSDME,从而抑制细胞焦亡。课题组进一步在类器官和各种小鼠模型中证实了甘露糖能够抑制GSDME介导的肠道或肾脏发生细胞焦亡,由此减轻一线化疗药顺铂或奥沙利铂引起的肠道或肾脏毒副作用;而在表达GSDME(T6A)突变体小鼠中,甘露糖则没有效果;但是甘露糖不会影响化疗药物对肿瘤的治疗效果。重要的是,在临床接受XELOX化疗方案的肿瘤患者出现腹泻以及粪便白细胞数显著增多等化疗副作用,而在补充甘露糖后,化疗副作用的表现则显著减轻。
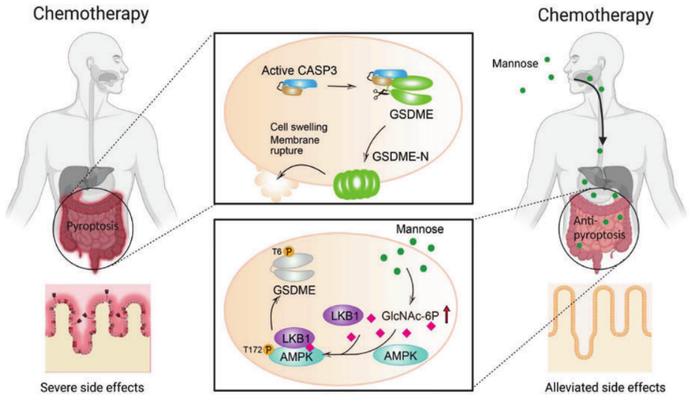
综上,该研究不仅揭示了甘露糖激活AMPK依赖于HBP中代谢物GlcNAc-6P的提高,AMPK激活可以磷酸化GSDMEThr6,导致caspase-3不能结合并剪切GSDME蛋白,引起焦亡抑制的新机制;而且在小鼠模型和临床患者中进一步证实了甘露糖可以减轻化疗药物引起的毒副作用,为临床减轻化疗副作用提供了新思路和新策略,具有很好的应用前景。
原文链接:https://www.nature.com/articles/s41422-023-00848-6

会议详情
会议名称:2023(第14届)细胞与基因治疗国际研讨会
暨抗体工程与创新免疫治疗技术论坛
暨2023细胞免疫治疗专业委员会年会
主办单位:生物谷、梅斯医学、同济大学附属同济医院、南京可缘
大会时间:9月22-23日
大会地点:上海
大会规模:1500人
2010年至今,生物谷联合各合作单位已经顺利召开了13届细胞与基因治疗国际研讨会,与全球致力于细胞治疗行业同仁们一同成长沉淀,在提供行业信息交流平台的同时,也为基础研究提供了技术/产品等产业化的孵化平台。
基于此,本届会议将继续以转化医学为切入点,以基础研究与临床应用相结合,针对细胞治疗的临床前沿研究、临床监管、治疗规范、细胞治疗安全性,免疫细胞新型疗法、实体瘤治疗、干细胞与癌症、抗体药物、核酸药物、基因编辑、肿瘤免疫治疗等热门议题进行讨论,诚邀国内外产学研医专家共聚,共绘产业发展新蓝图!
