速递!礼来在中国递交「度拉糖肽」新适应症上市申请
转自:医药观澜
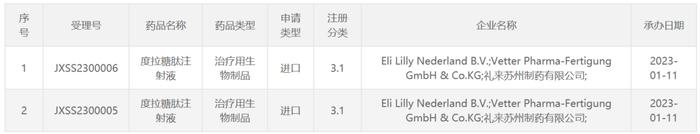
今日(1月11日),中国国家药监局药品审评中心(CDE)官网公示,礼来公司(EliLillyandCompany)申报了度拉糖肽注射液的新适应症上市申请。公开资料显示,度拉糖肽是一款长效GLP-1受体激动剂,每周给药一次,此前已在中国获批用于成人2型糖尿病。2022年7月,礼来宣布,度拉糖肽在一项于中国进行的3期临床试验中达到主要终点,用以支持在中国新适应症的申请,即联合胰岛素治疗成人2型糖尿病。
人胰高糖素样肽-1(GLP-1)是肠道细胞分泌的一种多肽类激素,它通过与GLP-1受体相结合,刺激胰岛素的分泌,并且抑制胰高血糖素的分泌,从而促进葡萄糖的代谢。同时,它还能够能起到延缓胃排空和抑制食欲的效果。天然的GLP-1在人们用餐之后,受到葡萄糖的刺激而分泌。而在2型糖尿病患者中,GLP-1的分泌水平显著下降,这也是导致患者血糖控制不佳的重要原因之一。
度拉糖肽是一种长效GLP-1受体激动剂,每周给药一次,可有效降低糖化血红蛋白(HbA1c)、适度减轻体重,此外它还具有低血糖风险低、免疫原性低的优势。度拉糖肽于2014年首次获美国FDA批准,目前它已在全球多地获批用于成人2型糖尿病患者的血糖控制,包括单药治疗及联合治疗。2020年2月,该药再次获得FDA批准用于患有心血管疾病或存在多种心血管风险因素的2型糖尿病成人患者,降低主要不良心血管事件(MACE)发生风险。
在中国,度拉糖肽于2019年获批上市,用于成人2型糖尿病患者的血糖控制,包括单药以及接受二甲双胍和/或磺脲类药物治疗血糖仍控制不佳的患者。

2022年7月,礼来宣布,度拉糖肽联合胰岛素治疗的3期AWARD-CHN3研究达到主要终点和所有关键次要终点。这是一项在中国进行的多中心、随机、双盲、平行组、安慰剂对照3期临床试验,针对的是接受稳定剂量甘精胰岛素(伴二甲双胍治疗和/或阿卡波糖)治疗血糖仍控制不佳的中国成人2型糖尿病患者,比较在滴定的甘精胰岛素治疗基础上,分别接受度拉糖肽1.5mg或安慰剂治疗的有效性和安全性。研究共纳入291例成人2型糖尿病患者,在中国27家研究中心完成。
该研究结果显示,在为期28周的AWARD-CHN3研究中,度拉糖肽联合滴定的甘精胰岛素治疗成人2型糖尿病,可显著降低2型糖尿病患者的HbA1c、体重及空腹血清葡萄糖。
2型糖尿病是影响全球2亿多患者的慢性代谢性疾病。患者的主要表现为胰岛素抵抗,导致胰岛素的功能不能得到充分发挥。对于这些患者来说,单纯使用胰岛素不能很好地改善患者病情,因此他们需要其它类型的降糖药物来控制血糖水平。
希望度拉糖肽新适应症上市申请尽快获得批准,早日惠及更多糖尿病患者。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.RetrievedJan10,2023.From https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c
[2]礼来宣布度易达®(度拉糖肽)联合胰岛素治疗III期试验AWARD-CHN3达到主要终点和所有关键次要终点.RetrievedJul12,2022,from https://mp.weixin.qq.com/s/_T-dH8DtEDRovL_Ktqr11A
