前沿 | 解决先导编辑体内递送瓶颈,刘如谦团队发布改良版病毒样颗粒载体
转自:药明康德
基因编辑技术展现了通过精确修正致病基因突变来治疗多种疾病的潜力。作为下一代基因编辑技术的代表,先导编辑(primeediting)技术的独特之处在于它仅对DNA的单链进行切割,从而避免了由双链DNA断裂引起的染色体缺失、重排等潜在风险,从而弥补了首代CRISPR技术的局限性。然而,将这些复杂的基因编辑工具有效地传递到活体动物的细胞中仍然是当前亟待解决的一个挑战。
近期,基因编辑领域知名学者刘如谦(DavidLiu)博士的研究团队在《自然》杂志子刊NatureBiotechnology上发表了一项开创性的研究。他们利用工程化的病毒样颗粒(VLPs)成功实现了先导编辑器的体内递送,并在一种遗传性疾病动物模型中取得了治疗效果。这项研究不仅展示了先导编辑技术的强大潜力,也为未来基于先导编辑技术的基因疗法提供了新的思路。

先导编辑技术代表了基因编辑领域的一项重大进展,它能够精确地将目标DNA序列替换为几乎任何其他特定序列,并能够实现特定DNA序列的插入或删除。这一技术的核心组件之一是将Cas9蛋白与逆转录酶(reversetranscriptase)融合形成的一种特殊蛋白。另一个关键的组成部分是名为“pegRNA”的特殊指导RNA(gRNA)。与传统gRNA不同,pegRNA不仅携带用于识别目标DNA序列的RNA,还包含了用于指导DNA序列修改的模板。
在先导编辑过程中,Cas9-逆转录酶融合蛋白在pegRNA的指引下,精确地切开一条DNA链,并依据pegRNA上的“修改模板”,合成含有修正序列的新DNA。此后,细胞的DNA修复机制会自动将这段新合成的序列整合入基因组。由于其独特的作用机制,先导编辑在减少非靶向编辑和旁观者编辑(bystanderediting)方面表现出明显的优势,并且在减少插入缺失产物或双链DNA断裂等其他非预期效应方面也显得尤为有效。这种机制的精确性和高效性,使得先导编辑技术在治疗遗传性疾病和进行基因组精准编辑方面显示出巨大的潜力。

为了充分发挥先导编辑技术在哺乳动物研究和治疗应用中的潜能,开发一种安全且高效的方法来准确地将先导编辑器递送到活体组织中至关重要。研究者们已经探索了多种递手段,目前处于临床试验阶段的体内基因编辑疗法主要采用腺相关病毒(AAVs)和脂质纳米颗粒这两种递送方式。然而,这两种方法各有不足:AAVs在递送负荷上受限且存在安全隐患;脂质纳米颗粒则主要在肝脏积聚,对其他器官的靶向作用有限。在此背景下,病毒样颗粒受到研究者的关注,它们由病毒的蛋白质外壳组成,能携带有效载荷但不包含病毒遗传物质。尽管如此,传统VLPs在体内递送效率通常有限,并且需针对不同有效载荷进行特定设计,以保证其能有效进入细胞。
在最新研究中,研究者们对工程化VLPs(eVLPs)及先导编辑器本身进行了全面优化和重新设计,以增强递送和编辑系统的效率。这一成果是基于刘如谦教授团队在2022年发表的一项研究,该研究采用eVLPs递送其实验室开发的另一种基因编辑器——碱基编辑器。在既往研究的基础上,研究人员改进了先导编辑器有效载荷在eVLPs中的封装方法,优化了有效载荷与递送载体的分离过程,并改良了将载荷有效输送至靶细胞核的途径。为了实现最佳编辑效果,研究人员强调,先导编辑器有效载荷必须在eVLPs颗粒形成时被有效地包装到eVLP中,而且在进入靶细胞后能够从颗粒中释放出来。这些步骤的精确协调和实施是保证eVLP介导的先导编辑高效性的关键。
研究团队进一步证实,装载有先导基因编辑组件的eVLPs能够有效地在活体小鼠大脑中实施基因编辑。在对大脑皮层进行的研究中,研究人员发现近一半接受先导编辑治疗的细胞展示了明显的基因编辑表型。
为了评估该递送系统在体内的递送效率和治疗效果,研究团队首先在小鼠模型中对该系统进行了测试,目标是纠正眼睛中的两种不同基因突变。其中一种基因是Mfrp,其突变会导致视网膜色素变性,这是一种导致视网膜进行性退化的遗传性疾病。另一种突变发生在Rpe65基因上,它与Leber先天性黑蒙相关,其突变也可能导致失明。在这两种情况下,经过基于eVLPs的先导编辑治疗后,约20%的小鼠视网膜细胞的突变得到了纠正,并在一定程度上恢复了视力。
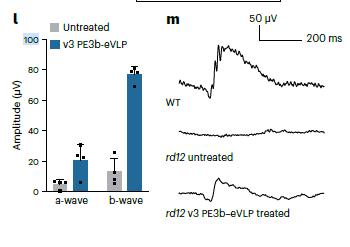
目前,用于基因编辑的病毒样递送系统尚未在人类中进行测试。在近期的一次采访中,刘如谦教授指出,未来基因编辑工具应以蛋白质形式传递,以最大限度地降低潜在副作用。目前,他的研究团队正致力于改进eVLPs,并计划在非人灵长类动物中进行测试,这对于进一步将这项技术应用于体内其他组织类型的靶向治疗具有重要意义。
综上所述,这项研究的成果不仅验证了eVLPs作为基因递送载体的高效性,还展示了其在神经科学研究和神经系统疾病治疗中的广泛应用潜力。eVLPs在复杂而敏感的大脑环境中实现了精准的基因编辑,为未来基因疗法的发展提供了新的可能性,并有望对治疗神经退行性疾病和遗传性神经病变产生深远影响。
