GZR101注射液II期成年2型糖尿病患者招募
转自:甘李药业

成年2型糖尿病患者招募
○项目介绍○
尊敬的患友们您好:
甘李药业目前正在进行一项“在口服降糖药控制不佳(A部分)或既往使用基础/预混胰岛素控制不佳(B部分)的2型糖尿病患者中比较GZR101注射液与德谷门冬双胰岛素注射液(诺和佳®)的疗效、耐受性和安全性的多中心II期临床研究”(临床试验登记与信息公示平台备案号:CTR20232521)。本研究现招募口服降糖药控制不佳或既往使用基础/预混胰岛素控制不佳的成年2型糖尿病患者,拟在全国约20家临床研究中心开展,预计总共招募120例患者。本研究已经获得国家药品监督管理局和医学伦理委员会的批准。
试验药物
GZR101注射液是甘李药业自主研发的1类新生物药,是新型预混双胰岛素复方制剂。相较于已上市的双胰岛素复方制剂,预期GZR101注射液在每日一次给药下能更好地模拟生理性胰岛素的分泌模式,GZR101注射液组分内基础和餐时两种胰岛素成分能够独立发挥作用,实现更安全有效地控制空腹和餐后血糖的目的。同时GZR101注射液降糖平稳,有望在提高血糖控制达标率的同时简化治疗,提高患者治疗依从性和降低治疗负担,优化糖尿病长期管理,降低或延缓糖尿病并发症的发生。
研究过程
本研究分为A和B两部分,每部分各两个治疗组,筛选合格的受试者随机进入GZR101注射液治疗组或德谷门冬双胰岛素注射液(诺和佳®)治疗组。所有受试者在随机后均接受标准的饮食和运动指导,给药周期16周,整个研究时间最长约21周。
我们将遵照要求对您的个人信息严格保密,研究期间您会获得研究医生对您疾病的科学指导和对您身体状况的密切医疗监测。与临床研究相关的有关诊疗、检查、化验均由申办方承担相应费用,同时您还将获得一定交通和营养补助。
入组标准
以下是受试者入组本临床试验的主要基本要求:
A/B部分共有
1.年龄为18至75周岁的中国成年人,男女不限;
2.临床确诊为2型糖尿病时间超过6个月;
3.连续3天(含随机当天)早餐前末梢血糖平均值小于等于13.9mmol/L,筛选时糖化血红蛋白(HbA1c)在7%至11%之间;
4.体重指数(BMI)在20至40kg/m2之间(计算方法:BMI=体重(公斤)/身高(米)的平方);
5.女性受试者须未孕;
6.同意在整个研究期内本人及伴侣采取有效的避孕措施;
7.1个月内没有参加其他的临床试验;
8.理解并遵守研究流程,自愿参加,并签署知情同意书。
仅A部分:
1.目前正在接收不超过3种类型的口服降糖药(必须包括二甲双胍),可联合或不联合的口服降糖药仅包括DPP4抑制剂、α-糖苷酶抑制剂、SGLT2抑制剂、葡萄糖激酶激活剂、磺脲类、格列奈类口服降糖药治疗,且保持药物剂量稳定至少3个月;
2.1年内胰岛素累积使用不超过2周,且3个月内未使用过胰岛素;
仅B部分:
1.目前正在接收不超过3种类型的口服降糖药,并联合1种基础胰岛素或预混胰岛素治疗(胰岛素每日给药频率不超过2次),且胰岛素治疗联合稳定剂量口服降糖药治疗至少3个月;
2.口服降糖药必须包括二甲双胍,可联合或不联合的口服降糖药仅包括DPP4抑制剂、α-糖苷酶抑制剂、SGLT2抑制剂、葡萄糖激酶激活剂、磺脲类、格列奈类。预混胰岛素不包括诺和佳®。
联系方式
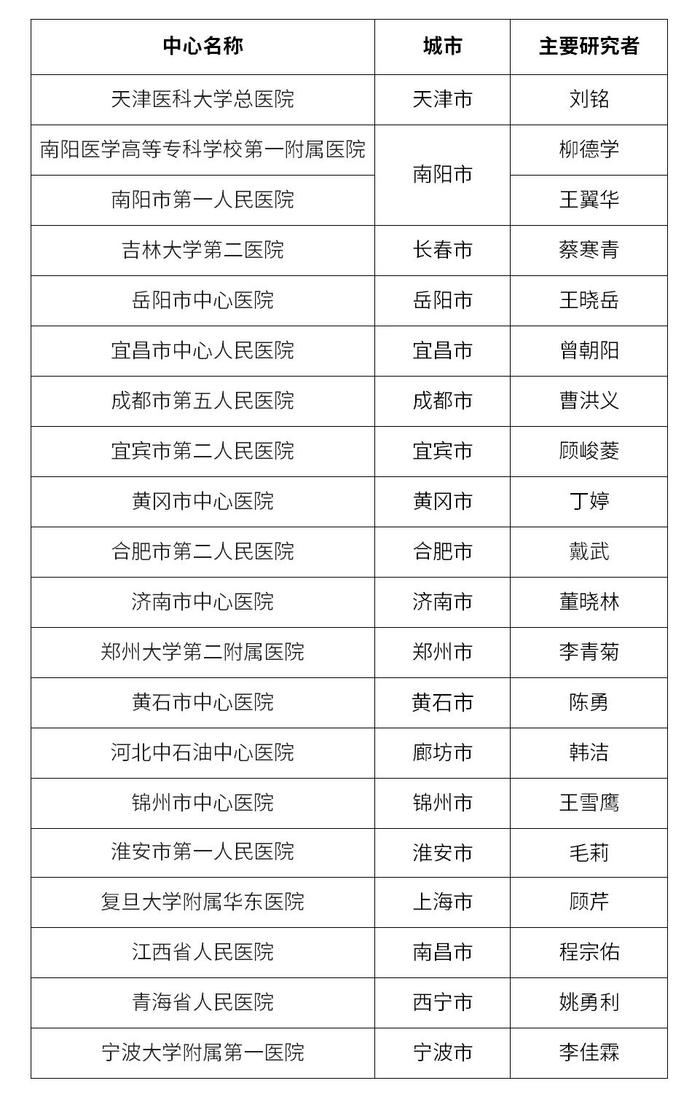
如果您有意愿参加本次临床试验,可联系黄老师(电话400-6759-099),咨询“甘李药业GZR101注射液临床试验项目招募”。您可就近选择方便的研究医院参与,研究中心列表如下(图片可点击放大查看):