Covid-19的积极影响:mRNA流感疫苗呼之欲出
转自:药渡
世卫组织总干事谭德赛博士5月5月宣布,肆虐全球数年,造成全球7亿6千多万人感染,以及将近7百万人死亡的Covid-19疫情结束。但这个官方宣布的结果并不代表Covid-19不再会对全球健康构成威胁。
就在我们认为Covid-19终于露出偃旗息鼓的迹象时,人类还要面对很多没有被征服的病毒,它们仍然定期或者不定期地卷土重来,威胁人类的健康安全。其中流感病毒就是这样的人类大患之一。每年都要肆虐的流感病毒传播都似洪水猛兽,造成大量的感染和死亡。全世界每年有50万人死于流感病毒。
1
mRNA流感疫苗
Covid-19的启示
人类面对流感的防御措施,目前主要建立在疫苗的开发方面。Covid-19疫情为流感疫苗开发提供了他山之石,辉瑞、Moderna以及其它流感疫苗的开发商,正在使用在Covid-19疫苗中获得成功的mRNA技术来开发和改进新一代的流感疫苗。第一批mRNA流感疫苗呼之欲出,它们的有效性要高于现有流感疫苗,后者的有效性可能低到只有20%左右(图1)。
本来如果乐观的话,mRNA疫苗有可能在2023年就能问世。但Moderna2月份公布的数据尚不足以令人额手相庆,他们在刚过去的4月份表示,需要继续研究疫苗直到数据足够令人振奋,这让人对其上市时间表产生了一些疑问。Moderna的竞争对手辉瑞的mRNA流感疫苗数据,有望在今年晚些时间发布。
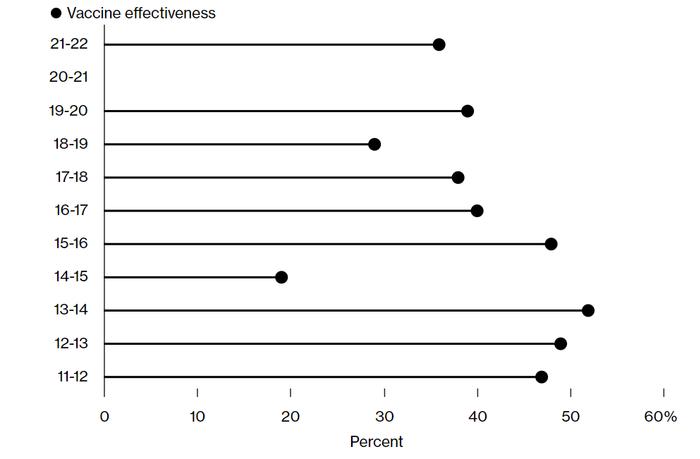
(数据来源:CentersforDiseaseControlandPrevention)
辉瑞和Moderna这两家在Covid-19中“扶摇直上九万里”的制药公司,据说去年共销售出了高达560亿美元的Covid-19疫苗,但2023年,这一数字可能将下滑至210亿美元。面对这个“一杯成喜亦成悲”的局面,这两大疫苗巨头需要提振他们下滑的销售额。而得到烈火检验的mRNA技术,恰好可以利用在流感疫苗的开发领域。而且它们想出了让Covid-19和流感疫苗比翼双飞的主意,将它们组团进行每年一次的注射。
在美国,流感疫苗的接种率约为50%,而最新的Covid疫苗的接种率为17%。通过将它们配对,更多的人可能会同时获得这两种疫苗,公司也可以实现更高的销售额。根据Jefferies分析师的说法,mRNA流感疫苗和Covid搭伙衍生出来的这个助推器组合,其全球市场价值可能达到每年500亿美元的水准。每剂组合的疫苗可以轻松实现100美元的出售价格。目前流感疫苗通常每针的花费约30美元。
除了辉瑞和Moderna之外,其他流感疫苗巨头,包括葛兰素史克、CSLSeqirus和赛诺菲,也正在厉兵秣马地进行自己的mRNA流感疫苗研发。Moderna正在测试五种流感疫苗,预计最终会有一种脱颖而出。流感全年传播,但通常在寒冷月份最为严重。流感疫苗的开发过程可能很漫长。
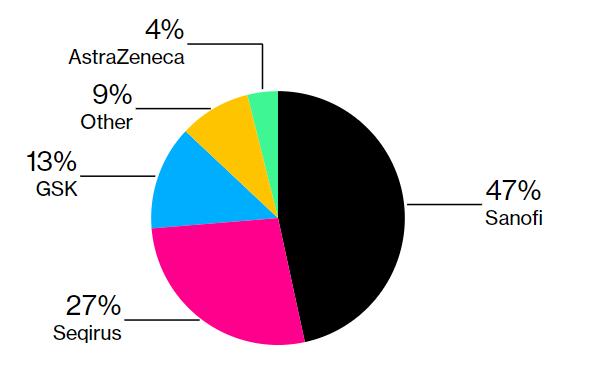
在世界卫生组织的指导下,一组科学家正在无悔追踪病毒,并在即将到来的流感季节前六个月告诉疫苗制造商哪些毒株最有可能“坏得冒尖”。从那时起,通常至少需要六个月的时间才能开发和生产所需的大量流感疫苗。[1]这是因为最常见的流感疫苗依赖于细胞生长,候选疫苗病毒被注射到鸡蛋中,并在鸡蛋中进行复制。[2]除了鸡蛋抗毒之外,还有两种其他类型的流感疫苗可供使用:即基于哺乳动物细胞(而非鸡蛋)的疫苗;以及在昆虫细胞中培养的重组流感疫苗。目前全球流感疫苗销售份额见图2。目前格局的三巨头是Sanofi,CSLSeqirus和GSK。
2
摆脱鸡蛋、赢得时间
mRNA疫苗的优势
流感疫苗制造商利用科学家提供的病毒信息每年生产出大约5亿支流感疫苗。它们大多的问世仍然通过已经存在了近九年的鸡蛋方法。该方法有两个主要弱点:
1)流感经常发生变异,研究人员有时会选错病毒;2)病原体还可以适应它生长的鸡胚胎,从而产生与制造商的目标疫苗在基因上存在不同的疫苗。这些变化并不危险,但也使得流感疫苗变得意兴阑珊。
在最近的一次流感疫苗注射中,美国的研究人员发现它可以将住院风险降低一半。根据疾病控制和预防中心的数据,流感疫苗的成功率约为36%。但常态是,在毒株预测不准的年份,流感疫苗有时候只能起到安慰作用,其势不能穿鲁缟。通常的有效率在40到60%之间。[3]
mRNA疫苗在Covid领域获取的部分成功,为流感疫苗的开发提供了新的思路。尽管mRNACovid注射只出现了几年左右,但mRNA的发现可以追溯到1960年代。mRNA疫苗不是使用病毒本身,而是使用病毒的遗传密码。mRNA翻译DNA中的遗传信息,指导人体数千种蛋白质的合成。如果能制造mRNA,理论上可以引导身体制造一种特定的蛋白质,例如SARS-CoV-2病毒的刺突蛋白,并刺激免疫系统针对性地量身定制,构建相应的防御系统(抗体)。
丰满的理想面临的第一个现实挑战,在于如何将mRNA递送到它能够起效的体内目标之中。科学家们开发了脂质纳米颗粒,这种特殊的脂肪球可以封装并隔离mRNA,以便让疫苗真正激活免疫系统。与基于鸡蛋的疫苗不同,mRNA疫苗的生产过程相对较快。它可以让世卫组织研究人员比正常情况晚三个月做出季节性流感预测,从而将预测与病毒实际传播之间的时间缩短一半,从而更加准确预测即将流传的病毒毒株,亦步亦趋地开发相应的流感疫苗。时间就是效率,这病毒预测的领域得到最切实的体现。
3
时不我待
巨头的mRNA流感疫苗开发
辉瑞和Moderna两家公司都表示,他们最早可以在明年将mRNA流感疫苗投放市场。为了获得FDA的批准,它们必须证明mRNA注射至少与现有产品一样好。投资者一直对Moderna发布的数据感到不满,每当它发布实验性流感疫苗的最新消息时,它的股价就会反受其累地下跌。[4]Moderna表示,他们已经消除了最初的小问题,而且动用集团军战术,同时测试另外四种疫苗,实现“必有一款适合您”的目标。
流感疫苗第二大巨头Seqirus自然也在mRNA的领域“弄潮儿向涛头立”。他们甚至更进一步,多年来一直在研究下一代mRNA技术:被称为自扩增信使RNA(sa-mRNA,self-amplifyingmRNA),并努力实现其商业化,作为一种可行的流感疫苗技术应用。sa-mRNA疫苗包括源自自我复制的单链RNA病毒的基因工程复制子,不仅有可能向免疫系统发出制造蛋白质的指令,而且还提供扩增mRNA的指令。[5] 这意味着sa-mRNA与等量的常规mRNA相比,sa-mRNA可以触发更多蛋白质的产生,以及更有效的细胞免疫反应。
这可能使疫苗制造商开发出剂量更小、反应原性率更低的更有效的疫苗,从而增强其在大流行和季节性环境中的价值。Seqirus已于2022年10月公布了令人振奋的sa-mRNA流感疫苗临床前数据,并将研究结果发表在MolecularTherapy–MethodsandClinicalDevelopment期刊上。数据表明,sa-mRNA候选流感疫苗对大流行和季节性流感毒株A(H5N1)和A(H1N1)产生了有效的交叉反应性免疫反应。[6]
遗祸无穷的Covid-19,在对全球造成惨重损失的同时,或许将催生mRNA疫苗的加速发展,凤凰涅槃一般地造福人类。
[1]CDC.SelectingVirusesfortheSeasonalInfluenzaVaccine.Availableat: https://www.cdc.gov/flu/prevent/vaccine-selection.htm Accessed06.05.2023.
[2]CDC.HowInfluenza(Flu)VaccinesAreMade.Availableat https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm Accessed06.05.2023.
[3]CDC.VaccineEffectiveness:HowWelldotheFluVaccinesWork?Availableat https://www.cdc.gov/flu/vaccines-work/vaccineeffect.htm. Accessed06.05.2023.
[4]Waldron,J.Moderna'smRNAflushotstrugglestoproveitsworthagaininphase3trial.FierceBiotech.11,04,2023.
[General]WhatDoesmRNAMeanfortheFluVaccine?Pfizer.Availableat:
https://www.pfizer.com/news/articles/what_does_mrna_mean_for_the_flu_vaccine Accessed06.05.2023.
[General]mRNACouldReinventVaccines.TheFluIsNext.Bloomberg.03.05.2023.
[5]Vigel,B.etal.Self-AmplifyingRNAVaccinesGiveEquivalentProtectionagainstInfluenzatomRNAVaccinesbutatMuchLowerDoses.AmericanSocietyofGene&CellTherapy.2018.10.1016
[6]Chang,C.,etal.Self-amplifyingmRNAbicistronicinfluenzavaccinesraisecross-reactiveimmuneresponsesinmiceandpreventinfectioninferrets.MolecularTherapy–MethodsandClinicalDevelopment.2022,27,195-205.
