儿童抗肿瘤药物临床研发技术指导原则,自发布之日起施行
2023-03-24 18:54:58 - 市场资讯
转自:蒲公英Ouryao
2023年03月24日,国家药品审评中心发布了《儿童抗肿瘤药物临床研发技术指导原则》,自发布之日起施行。
重点内容
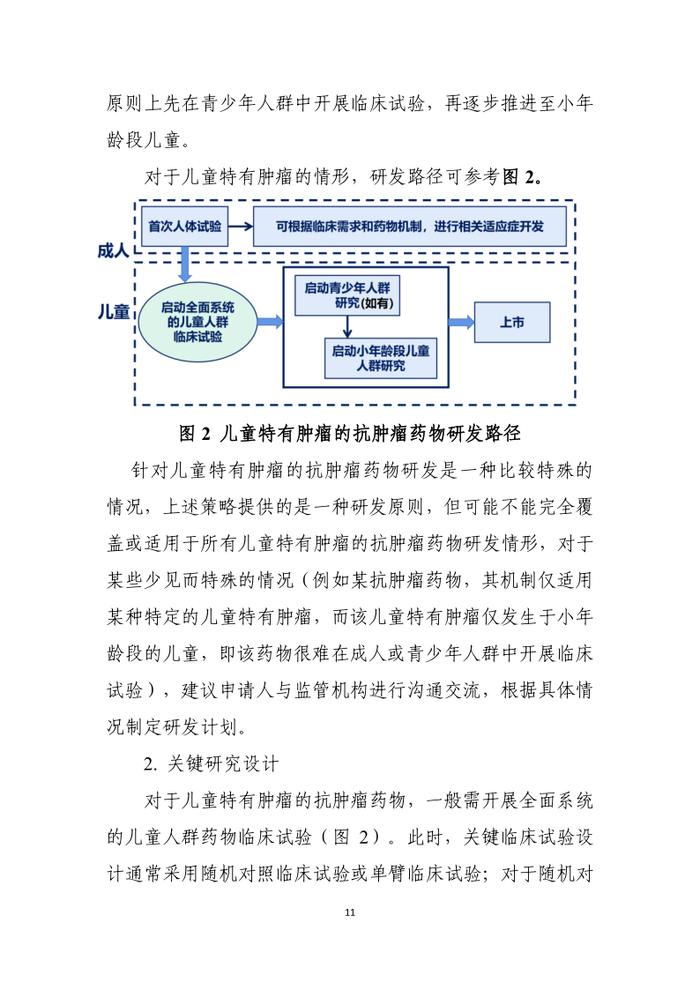
一般情况下,遵循儿童药物研发的普遍规律,按成人-青少年-小年龄段儿童的年龄顺序,逐步推进研发;
与成人临床试验相比,儿童人群临床试验在伦理学考虑、知情同意、筛选与入组操作和评价方法等诸多方面更具挑战,在儿童人群中开展大规模的临床试验难度更大;
儿童抗肿瘤药物研发中,可借鉴的数据通常来自于成人人群的临床研究中产生的药代动力学、药效学、疗效及安全性数据;
通过数据外推,可减少或豁免部分儿童临床试验,或优化儿童人群临床试验[4];
儿童药物临床试验“试错”的可接受程度往往更低,因此在启动儿童人群临床试验时,通常只有在对其临床获益有充分预期的情况下,让儿童患者暴露于试验药物的风险才可被接受;
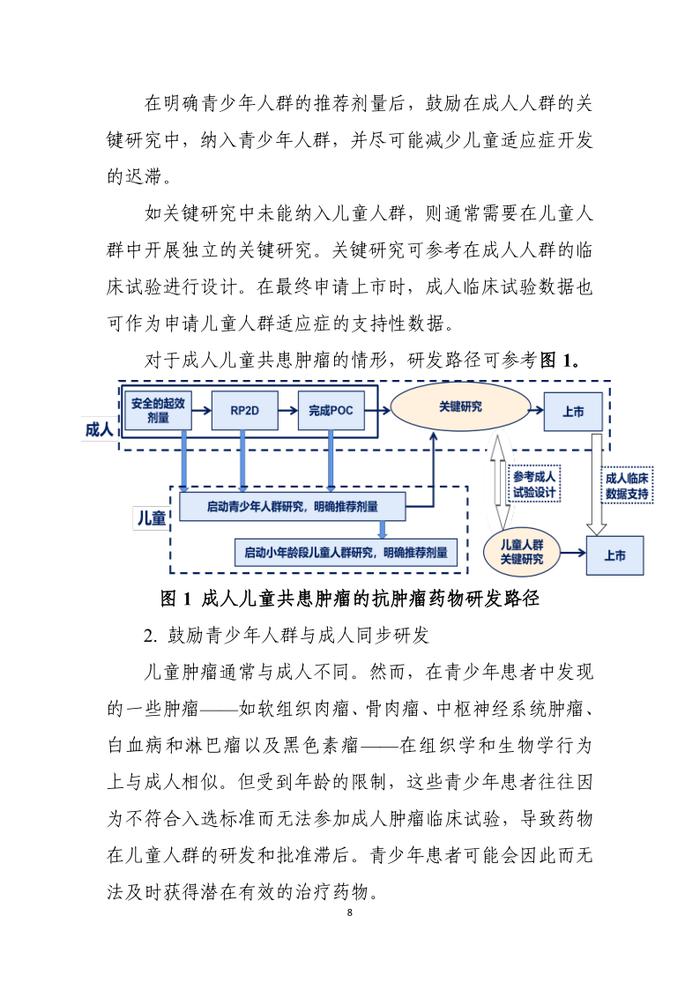
如关键研究中未能纳入儿童人群,则通常需要在儿童人群中开展独立的关键研究;
主要内容

为了对儿童抗肿瘤新药的临床研发提供思路和技术建议,药审中心组织撰写了《儿童抗肿瘤药物临床研发技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行,原文如下: