Science | 发现一系列针对 SARS-CoV-2的强效抗病毒氨基吡啶先导化合物
转自:生物谷
在一项新的研究中,来自COVIDMoonshot联盟的研究人员发现了一系列针对SARS-CoV-2的强效抗病毒氨基吡啶先导化合物,比如MAT-POS-e194df51-1。它还反映了其开放科学方法在启动一项无专利的抗病毒药物发现计划方面的成功。相关研究结果发表在2023年11月10日的Science期刊上,论文标题为“OpensciencediscoveryofpotentnoncovalentSARS-CoV-2mainproteaseinhibitors”。

COVIDMoonshot计划始于2020年3月的一次自发虚拟合作,当时一群来自学术界和生物制药界的科学家和学生在推特呼吁的推动下,联手开始了一场争分夺秒的竞赛,以确定可以阻止SARS-CoV-2病毒的新分子。
这项史无前例、众筹和完全开放的合作由200多名科学家参与,他们迅速鉴定并开发出了新型化合物,这些化合物对SARS-CoV-2冠状病毒的一种关键酶---主蛋白酶(mainprotease,Mpro)具有极佳的抗病毒活性。
COVIDMoonshot联盟如今与“被忽视疾病药物倡议(DrugsforNeglectedDiseaseinitiative,DNDi)”合作对这些先导化合物进行临床前评估。COVIDMoonshot联盟致力于发现安全的、全球负担得起的抗病毒药物,以对抗COVID-19和未来的病毒大流行,并开创了一种直接仿制的无专利方法。
这篇论文报告了一种非共价、非肽抑制剂支架的发现,该支架具有类似先导药物的特性,有别于目前的主蛋白酶抑制剂。他们的方法利用了众包、机器学习、超大规模分子模拟以及高通量结构生物学和化学。
它基于大流行开始时在钻石光源(DiamondLightSource)的XChem设施进行的一项大型实验的数据,该实验使用钻石光源的高通量晶体学进行晶体片段筛选。在该实验中,在数周内筛选出了1495个浸泡在片段中的晶体,确定了78个密集分布在酶活性位点的片段。
这些作者得以绘制出SARS-CoV-2主蛋白酶结构可塑性的详细图谱、多种化学型(chemotype)的广泛结构-活性关系以及丰富的生化活性数据。这次研究活动的所有化合物设计(>18,000个设计)、晶体学数据(>840个配体结合X射线结构)、检测数据(>10,000个测量)和合成分子(>2,400个化合物)都得到了快速和公开的共享,从而为未来的抗冠状病毒药物发现建立了一个丰富的开放和无知识产权的知识库。
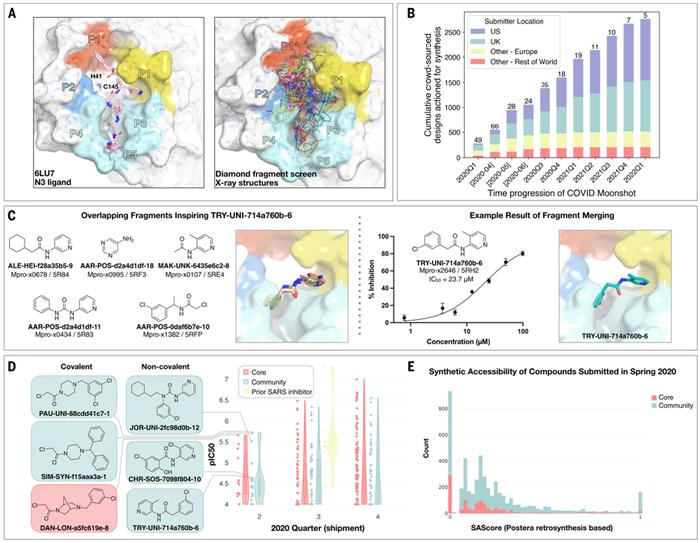
众包通过合并片段来快速识别化学型支架。图片来自Science,2023,doi:10.1126/science.abo7201。
作为这一系列强效的SARS-CoV-2抗病毒先导化合物中的一个例子,这些作者讨论了化合物MAT-POS-e194df51-1的抗病毒功效、吸收、分布、代谢和排泄以及药代动力学特征。MAT-POS-e194df51-1在多个细胞系的SARS-CoV-2抗病毒实验中表现出的中位有效浓度(EC50)在A549-ACE2-TMPRSS2细胞中为64nM,在HeLa-ACE2细胞中为126nM,没有明显的细胞毒性。这与这类氨基吡啶先导化合物的整体细胞功效相符:在A549-ACE2-TMPRSS2细胞病理效应测试中评估的150种酶测定后半数抑制浓度(IC50)<500nM的化合物中,有15种化合物的EC50值低于作为内部对照的奈玛特韦(nirmatrelvir),奈玛特韦在这种抗病毒实验中的EC50值为218nM。同样地,MAT-POS-e194df51-1在不同实验室和细胞系的“众包”抗病毒实验中也测得了良好的抗病毒活性,包括使用p-gp抑制剂和不使用p-gp抑制剂以及使用nirmatrelvir作为内部对照的抗病毒实验。
这些作者还观察到他们的先导化合物MAT-POS-e194df51-1对已知的SARS-CoV-2变体Alpha、Beta、Delta和Omicron具有良好的交叉反应性。与这种先导化学物密切相关的分子PET-UNK-29afea89-2和MAT-POS-932d1078-3在HeLa-ACE2细胞病理效应测试中的EC50值分别为240nM和331nM,在A549-ACE2-TMPRSS2细胞病理效应测试中的EC50值分别为657nM和2.57μM。MAT-POS-e194dfM在A549-ACE2-TMPRSS2细胞病理效应测试中的值分别为657nM和2.57μM,显示细胞内病毒RNA和感染性病毒分泌到人类诱导性多能干细胞(iPSC)衍生的肾脏类器官(图S16,D和E)顶端区室的数量减少了>100倍。MAT-POS-e194df51-1表现出口服生物可用性抑制剂所需的良好特性。
此外,晶体学研究显示,MAT-POS-e194df51-1与SARS-CoV-2主蛋白酶结合位点的相互作用模式与已获批准的主蛋白酶抑制剂奈玛特韦和恩司特韦(ensitrelvir)截然不同,可能具有互补的耐药性特征,因此有理由进一步开发。
论文共同第一作者、英国牛津大学药物发现中心团队负责人LizbeKoekemoer博士说,“这篇论文中的数据集提供了一个独特的资源,将全面的结构数据、片段筛选、多种化学支架以及生化和细胞检测数据联系起来,可供其他科学家查看和利用。”
论文共同第一作者、钻石光源高级光束线科学家、XChem设备负责人DarenFearon博士补充说,“这是首次为药物发现活动生成如此大量的蛋白配体结构并在公共领域发布。这不仅证明了钻石光源的高通量晶体学基础设施,也证明了全球众多研究小组在巨大压力下的惊人协调能力。”
论文共同通讯作者、钻石光源首席光束线科学家、牛津大学结构化学生物学教授FrankvonDelft教授说,“开放科学改变了生物科学的许多领域。COVIDMoonshot联盟为开放科学早期药物发现提供了一条可行的途径,从而推动了传染病药物发现的发展,这是一个对公众具有重大意义的研究领域,但私营部门对该领域的资助却长期不足。以冠状病毒主蛋白酶为作用靶标的COVIDMoonshot结构驱动药物发现活动为未来抗病毒药物的潜在开发提供了路线图。”
论文共同通讯作者、牛津大学的AnnettevonDelft博士补充说,“这篇论文展示了众包可以为药物发现带来的巨大价值。COVIDMoonshot项目的合作方式和对开放科学的承诺是独一无二的,它展示了合作如何成为创新的驱动力。”
随着COVIDMoonshot计划自发形成的这种药物发现平台合作如今继续作为ASAP(AI-drivenStructure-enabledAntiviralPlatform,人工智能驱动的结构化抗病毒平台)发现联盟开展工作,旨在发现和开发针对冠状病毒、黄病毒和肠道病毒的新型广谱小分子抑制剂,以应对大流行。
参考资料:
MelissaL.Bobyetal.OpensciencediscoveryofpotentnoncovalentSARS-CoV-2mainproteaseinhibitors.Science,2023,doi:10.1126/science.abo7201.
First-evercrowd-sourcedsmallmoleculediscoveryandapotentSARS-CoV-2antiviralleadcompoundhttps://medicalxpress.com/news/2023-11-first-ever-crowd-sourced-small-molecule-discovery.html
