ADC药物输注的标准与规范——《乳腺癌抗体偶联药物输注管理专家共识》
转自:医学界
ADC药物兼具抗体药物的精准靶向作用和细胞毒药物的高效杀伤优势,逐渐改变乳腺癌的治疗格局。目前,已经进入中国临床实践的ADC药物包括恩美曲妥珠单抗(T-DM1)、德曲妥珠单抗(T-DXd)和戈沙妥珠单抗(SG)等多个产品。T-DM1是首个获批用于实体瘤的HER2靶向ADC,基于III期EMILIA研究获批用于HER2阳性晚期乳腺癌的二线治疗,后根据KATHERINE研究获批用于新辅助治疗后non-pCR的HER2阳性早期乳腺癌辅助治疗[1,2]。T-DXd在DESTINY-Breast03研究中取得突破性结果,支持T-DXd作为HER2阳性晚期乳腺癌二线治疗新的标准方案[3]。此外,DESTINY-Breast04研究中T-DXd针对HER2低表达乳腺癌可显著延长PFS和OS(相比化疗),使得乳腺癌告别了HER2阳性和阴性的二分法时代,拓宽抗HER2治疗的获益人群[4]。SG则是首个上市的TROP2靶向ADC药物,为三阴性乳腺癌患者提供了重要治疗选择[5]。
新药不断上市的同时,也对医护人员使用ADC药物输注操作规范也提出新的要求。中国医药教育协会乳腺癌个案管理师分会专家组制订出《乳腺癌抗体偶联药物输注管理专家共识》(以下简称《共识》)[6],以T-DM1、SG以及T-DXd为例,全面阐述乳腺癌ADC药物的输注规范、相关不良反应的早期预防和及时管理的实践指导,以供医护人员对乳腺癌ADC药物静脉输注操作规范进行参考。

乳腺癌ADC药物配置、输注标准操作流程(SOP)
《共识》强调乳腺癌ADC药物静脉输注应遵循现用现配、无菌配置原则,配置流程见图1;配置过程中严格执行查对制度,双人核对、确认后,单双人签字;建议在静脉药物配置中心(PIVAS)实行集中调配和供应,或在病房内具有生物安全柜或超净工作台条件下进行配置,以期降低毒性药物对医护人员的职业伤害。输注过程遵循静脉输液流程,见图2。
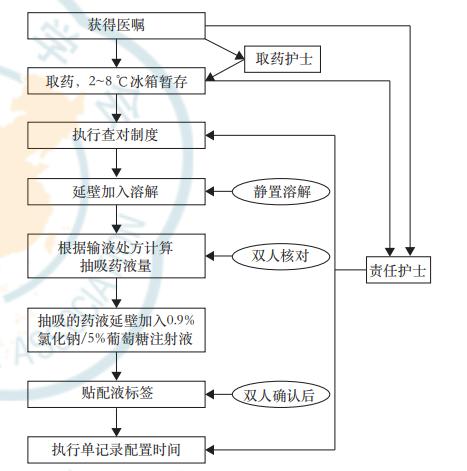
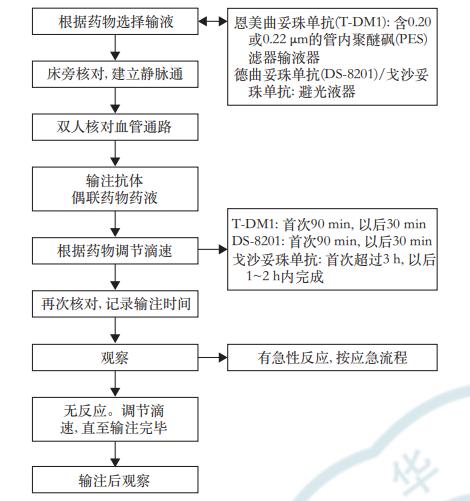
ADC药物输注过程中,如果患者发生输注反应,应采取以下应急预案:(1)患者自我感知到最容易发现的反应,告知护士,或护士巡视中询问/观察发现;(2)立即关闭输液器,呼叫其他医务人员协助;(3)更换输液器,回抽留置针内药液,办公室护士协助保存余药、确认医师知晓、携抢救用品到床边;(4)做好抢救准备,遵医嘱用药,观察患者,寒战患者注意保暖,监测体温;(5)详细记录:抢救过程、生命体征、开始及结束时间等;(6)做好复输准备,反应严重的禁止复输;(7)丢弃的药物按余药处理流程进行(图3)。
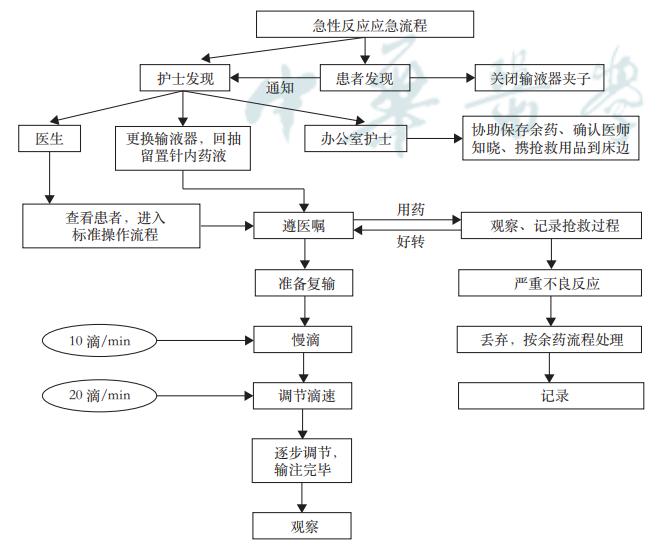
乳腺癌ADC药物输注管理
1.ADC药物规格及配置原则
《共识》指出,T-DM1(100mg/瓶和160mg/瓶)、T-DXd(100mg/瓶)和SG(180mg/瓶)虽同属ADC药物,但3种药物的分子结构特性各不相同,不能相互替换或者联用,为了防止用药错误,输注前应仔细检查、核对西林瓶标签,以确保正在制备和使用的药物正确。药物的配置和用法、用量应严格按照医嘱和使用说明书的要求执行。
2.ADC药物注射液配置及给药方案
《共识》分别阐述了T-DM1、T-DXd和SG的注射液配置流程以及给药方案。需要强调是,T-DM1不应使用葡萄糖(5%)溶液,其会引起蛋白质聚集;也不得与其他药物混合或稀释。T-DXd不可使用0.9%氯化钠溶液进行稀释,其可能会导致颗粒形成。SG只能使用0.9%的氯化钠溶液配置,不能将SG替换成含有伊立替康或其活性代谢物SN-38的其他药物,或与此类药物联用。并且,ADC药物输注前应监测血常规、血生化等指标,输液中严密观察是否有发热、寒战等输液反应,输液后根据观察时间监测不良反应。
▌T-DM1的注射液配置及给药方案
(1)复溶溶液的配置:①使用无菌注射器,将5ml无菌注射用水缓慢注入100mg的T-DM1西林瓶中,或将8ml无菌注射用水注入160mg的T-DM1西林瓶中。②轻轻旋转西林瓶直至完全溶解,切勿用力甩动。③在2~8℃下贮藏复溶的T-DM1溶液;24h后丢弃未使用T-DM1溶液(复溶制剂仅供一次性使用,未用完部分应及时销毁)。④复溶溶液使用前应进行外观检查,确保无微粒物质或者变色。通常情况下,复溶溶液无可见微粒,为澄清至微乳光溶液。复溶溶液的颜色应为无色至浅棕色。如果复溶溶液含有可见微粒、浑浊或变色,则请勿使用。
(2)复溶溶液稀释说明:①从西林瓶中取出适量的溶液,然后将其添加到含有250ml0.45%氯化钠或0.9%氯化钠的输液袋中。②一旦做好输注准备,则应立即给药。③如果不立即使用,输注液可在2~8℃的冰箱中贮藏最多24h。④贮藏期间切勿冷冻或甩动输注袋。
(3)给药方案:①T-DM1推荐剂量为3.6mg/kg,1次/3周(21d为1个周期)。给予起始剂量时采用90min静脉输注,在输注期间应观察患者,并于初始剂量给药后至少90min内观察发热、寒战或其他输液相关反应。给药期间应密切监测输注部位,防止可能出现皮下外渗的情况。如果既往输注时的耐受性良好,则给予T-DM1的后续剂量时可采用30min输注。如果患者出现输注相关症状,应减慢本品的输注速率或中断给药。出现危及生命的输液反应时,应终止治疗。②T-DM1的典型不良反应剂量调整:T-DM1引起的血小板减少不良事件剂量调整如表1所示。
表1.T-DM1引起的血小板减少不良事件剂量调整

▌T-DXd的注射液配置及给药方案
(1)T-DXd的复溶液配置:①从储存中取出配制计划剂量所需数量的T-DXd药瓶,T-DXd溶液制备完成之前,需保留外包装盒。②取下无菌注射用水的盖子,并用酒精擦拭干净顶部。③每瓶T-DXd使用无菌注射器缓慢注入5ml无菌注射用水。④通过旋转、翻转小瓶使瓶中粉末充分溶解,不可摇晃。⑤配制成的溶液为无色至淡黄色的透明液体,最终浓度为20mg/ml。⑥溶解后的复溶液如果没有马上使用,最多可在2~8℃冰箱中保存24h,不可冰冻。⑦复溶制剂不含防腐剂,仅供一次性使用。
(2)T-DXd的复溶液稀释:①使用无菌注射器从西林瓶中取出计算出的量。检查复溶溶液是否有颗粒和变色。溶液应清澈无色至浅黄色。如果观察到可见颗粒或溶液混浊或变色,请勿使用。②将计算过体积的复溶的本品加入到含有100ml5%葡萄糖溶液的输液袋中进行稀释,不得使用氯化钠溶液。建议使用由聚氯乙烯或聚烯烃(乙烯和聚丙烯的共聚物)制成的输液袋。③轻轻翻转输液袋以充分混合溶液,请勿振摇。T-DXd制备以及给药期间,制备好的输液袋必须避光。④丢弃西林瓶中所有未使用的部分。
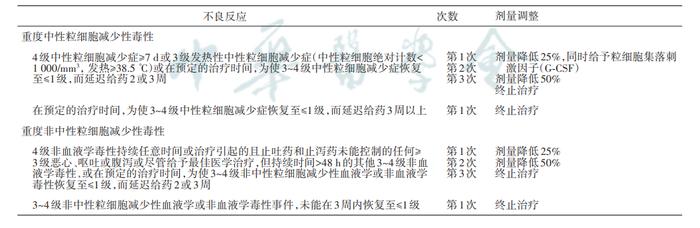
(3)T-DXd的给药方案:①T-DXd推荐剂量为5.4mg/kg,采用静脉输注给药(请勿静推或静脉快速避光注射)。1次/3周(每周期21d)静脉输注,直至疾病进展或出现无法耐受的毒性。首次输液:第1次滴注不少于90min;后续输注:如果耐受性良好,第2次起滴注不少于30min。如果患者出现输液相关症状,应减慢本品的输注速率或中断给药。出现严重输液反应时,应永久停用本品。②T-DXd典型不良反应剂量调整:T-DXd发生输注不良反应时,可能需要暂时停药、减少剂量或永久停药。针对不良反应,T-DXd推荐剂量减量,减少剂量后,请勿重新增加T-DXd剂量。T-DXd剂量降低方案为起始剂量5.4mg/kg,第1次减量调整为4.4mg/kg,第2次减量调整为3.2mg/kg,如需要进一步减量调整则终止治疗。T-DXd剂量及不良反应见表2。
表2.T-DXd不良反应剂量调整

▌SG的注射液配置及给药方案
(1)SG复溶溶液的配置:①使用无菌注射器,缓慢将20ml0.9%氯化钠注射液注入180mg的SG西林瓶中,得到浓度为10mg/ml的溶液。②轻轻旋转西林瓶,使其溶解15min,切勿用力甩动。③配置好的复溶溶液应立即进行稀释配置。④复溶溶液给药前,应目视检查注射药物中是否有颗粒物和变色现象。溶液应无可见微粒,呈澄清的黄色。如果复溶溶液浑浊或变色,请勿使用。⑤复溶后立即制备本品稀释溶液用于输注。
(2)SG复溶溶液稀释说明:①用注射器从西林瓶中取出适量的溶液,根据需要用0.9%氯化钠输注液调整输液袋中的体积,以使溶液浓度达到1.1~3.4mg/ml(总体积不应超过500ml),仅可使用0.9%氯化钠稀释进行输注。②如果体重超过170kg的患者,将SG总剂量均分于两个500ml的输液袋中,按顺序缓慢输注。复溶制剂仅供一次性使用,未用完部分应及时销毁。③一旦做好输注准备,则应立即使用输注袋中的稀释溶液,输液袋应避光。④如果不立即使用,输注液可在2~8℃的冰箱中贮藏4h。冷藏保存后,稀释溶液应在6h内(包括输注时间)使用完。⑤贮藏期间切勿冷冻或甩动输注袋,并且需避光。
(3)SG给药方案:SG的推荐剂量为10mg/kg,给药剂量不得超过10mg/kg。每21d为一个治疗周期,第1天和第8天静脉输注。一直持续治疗,直至出现疾病进展或不可接受的毒性。首次输注:输注时间应持续3h以上,在输注过程中和输注结束后至少30min观察患者是否出现输液反应。后续输注:如果之前输注可耐受,则输注时间可以为1~2h以上。在输注过程中观察患者是否出现输液反应,并在输注结束后观察至少30min。如果患者发生输液反应,需减慢本品的输注速率或中断本品输注。发生危及生命的输液反应时永久停用本品。在因不良反应降低剂量后,请勿重新上调剂量。暂停或永久停用SG的剂量调整见表3。
表3.SG不良反应的剂量调整
3.输液装置和输液通路的选择、ADC药物的保存
《共识》建议ADC药物优先选择经外周静脉置入的中心静脉导管(PICC)或输液港进行输注。不同ADC药物需使用不同的输液装置:T-DM1如果使用0.9%氯化钠进行输注,则需要0.20或0.22μm的管内聚醚砜(PES)滤器;T-DXd输液袋可使用聚氯乙烯、聚乙烯或者聚丙烯材质,过滤器仅可使用0.20或0.22μm的PES或聚砜(PS)过滤器;SG输注时使用常规输液器即可。
在配置和输注时,T-DXd和SG的输液袋和输液器均需避光。如果已制备的T-DXd输注液贮藏于冰箱中(2~8℃),应将输注液在避光条件下回温至室温再给药。《共识》详细介绍了3种ADC药物不同状态下的保存条件,见表4。
表4.乳腺癌ADC药物未开封、复溶和稀释溶液3种状态下的保存条件

4.ADC药物输注前预防用药
《共识》推荐采取以下措施预防ADC药物相关不良反应的发生:
T-DXd:具有致吐性[包括迟发性恶心和(或)呕吐],每次使用前应预先使用两种或三种药物组合[例如,地塞米松与5-HT3受体拮抗剂和(或)NK1受体拮抗剂,以及其他适用的药物],用于预防化疗引起的恶心和呕吐。
SG:每次SG输注前,建议预先使用退烧药、H1和H2阻滞剂,既往有输注反应的患者可使用糖皮质激素来预防“输液反应”;预先使用两种或者三种药物联合治疗方案(例如:地塞米松与5-HT3)预防恶心和呕吐。
T-DM1:输注前无需预防用药。
在未使用/过期药品的销毁、给药延迟或者漏用处理原则方面,《共识》也给出了详细建议。另外,为保证患者用药安全,应向患者进行自身情况评估、遵医嘱按时复查和常见不良事件反应注意和观察等宣教,嘱咐患者不适应及时报告医生。乳腺癌ADC药物输注常见不良反应的患者健康教育也是护理人员的工作内容之一,包括血液系统不良反应、输注反应、周围神经病变、肺毒性、消化道不良反应、心脏毒性等。
总结
《乳腺癌抗体偶联药物输注管理专家共识》从药物使用SOP、输注管理到健康宣教,通过16条推荐意见,有效地回答了护理人员在乳腺癌ADC药物输注过程中的主要问题,为临床实践提供了全面而详尽的指导,有助于提高乳腺癌患者在ADC药物输注过程中的安全性和治疗效果。
附16条《乳腺癌抗体偶联药物输注管理专家共识》推荐意见:
推荐意见1:乳腺癌ADC药物输注应遵循现用现配、无菌配置原则,配置过程中严格执行查对制度,双人核对、确认后,单双人签字(共识度:100%)。
推荐意见2:根据临床需要,乳腺癌ADC药物建议在静脉药物配置中心(PharmacyIntravenousAdmixtureService,PIVAS)实行集中调配和供应,或在病房内具有生物安全柜或超净工作台条件下进行配置,以期降低毒性药物对医护人员的职业伤害(共识度:98%)。
推荐意见3:ADC药物输注SOP遵循静脉输液流程(共识度:100%)。
推荐意见4:药物输注过程中,如果患者发生输注反应,应立即采取急性反应应急流程(共识度:99%)。
推荐意见5:建议T-Dxd和SG在药物避光配置(共识度:97%)。
推荐意见6:T-DM1、T-DXd及SG3种ADC药物必须严格按照无菌技术进行溶解配置与稀释,不能相互替换或者联用,为了防止用药错误,输注前应仔细检查、核对西林瓶标签,以确保正在制备和使用的药物正确;药物的配置和用法、用量应严格按照医嘱和使用说明书的要求执行(共识度:100%)。
推荐意见7:ADC药物输注建议优先选择PICC/输液港(共识度98%)。
推荐意见8:如果使用0.9%氯化钠进行T-DM1输注,则需要0.20或0.22μm的管内PES滤器;T-DXd过滤器仅可使用0.20或0.22μm的PES或PS过滤器;SG输注时使用常规输液器即可(共识度:99%)。
推荐意见9:T-DXd和SG输注时输液袋需避光;建议输液装置也需选择避光,输注时尽量关闭窗帘和灯光(共识度:98%)。
推荐意见10:T-DM1和T-DXd输注液可在2~8℃的冰箱中贮藏长达24h;SG输注液可在2~8℃的冰箱中贮藏最多4h,冷藏保存后,应在6h内(包括输注时间)使用完(共识度:98%)。
推荐意见11:T-DXd和SG具致吐性[包括迟发性恶心和(或)呕吐],每次使用前应预防用药(共识度:100%)。
推荐意见12:T-DM1不应使用葡萄糖(5%)溶液稀释,其会引起蛋白质聚集;不得与其他药物混合或稀释。T-DXd不可使用0.9%氯化钠溶液进行稀释,其可能会导致颗粒形成;SG只能使用0.9%的氯化钠溶液配置,请勿将SG替换成含有伊立替康或其活性代谢物SN-38的其他药物,或与此类药物联用(共识度:100%)。
推荐意见13:如果计划用药延迟或漏用,请尽快给药,无需等到下一个计划的周期;下次给药时,调整给药时间表,按正常间隔给药,以维持两次给药之间的3周间隔;以患者在最近一次输液中耐受的剂量和速率进行输液(共识度:97%)。
推荐意见14:ADC药物输注前应监测血常规、血生化等指标,输液中严密观察是否有发热、寒战等输液反应,输液后根据观察时间监测不良反应(共识度:98%)。
推荐意见15:为保证患者用药安全,应向患者进行自身情况评估、遵医嘱按时复查和常见不良事件反应注意和观察等宣教,嘱咐患者不适及时报告医生(共识度:100%)。
推荐意见16:需对患者进行输注常见不良反应的健康宣教,包括血液系统不良反应、输注反应、周围神经病变、肺毒性、消化道不良反应、心脏毒性等(共识度:97%)。
参考文献:
[1]SunilVermaetal.NEnglJMed2012;367:1783-91.
[2]G.vonMinckwitzetal.NEnglJMed2019;380:617-28.
[3]SaraAHurvitzetal.Lancet2023;401:105–17
[4]S.Modietal.NEnglJMed2022;387:9-20.
[5]A.Bardiaetal.NEnglJMed2021;384:1529-41.
[6]中国医药教育协会乳腺癌个案管理师分会.乳腺癌抗体偶联药物输注管理专家共识[J].中华医学杂志,2023,103(34):2704-2712.
该材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批编号:CN-124518 有效期至: 2024-11-21
