一定要等九价吗?首个国产二价HPV疫苗头对头试验数据公布
“现在在中国的市场上,HPV疫苗对9-45岁女性的渗透率不到12%,这意味着88%的女性在‘裸奔’,因为有性行为,就有存在感染HPV的机会。所以女性不是打九价HPV疫苗更重要,而是打疫苗更重要。”
5月5日,在厦门万泰沧海生物技术有限公司(以下简称“厦门万泰”)举办的首届媒体开放日上,厦门万泰董事长李世成说。厦门万泰沧海生物技术有限公司是国内知名企业“养生堂”旗下北京万泰生物药业股份有限公司(万泰生物,603392.SH)疫苗板块的骨干企业。
人乳头瘤病毒(HPV)可导致宫颈癌,2020年全球约60.4万人被诊断为宫颈癌,34.2万人因宫颈癌死亡。据介绍,目前已分离出的HPV达100多亚型,其中HPV16、18亚型诱发癌变的潜力最大。据中国医学科学院乔友林教授团队的研究,HPV16、18亚型在宫颈鳞癌患者的致病HPV(宫颈鳞癌在宫颈癌中的总体占比不低于90%)中约占84.5%。接种人乳头瘤病毒(HPV)疫苗是预防宫颈癌的重要手段。
2019年底,由厦门大学夏宁邵团队和养生堂厦门万泰共同研发的首个国产二价人乳头瘤病毒疫苗(大肠杆菌)(商品名:馨可宁®)获批上市,打破了国际大厂对国内HPV疫苗市场的垄断。馨可宁®覆盖的亚型为HPV主要致病亚型即为HPV16、18,该疫苗现已纳入全国多地的疫苗接种优惠政策。
馨可宁®的有效性和安全性如何?应如何选择HPV疫苗?开放日现场,相关专家对此进行了解释。
一项头对头试验数据公布
馨可宁®上市已超三年,近日,一项头对头试验数据公布。“头对头试验”是指非安慰剂对照试验,即采用临床上已经使用的药物或治疗方法作为对照进行的临床试验,可看作是两种药物在有效性和安全性上的直接比较。
据馨可宁®临床试验负责人之一、厦门大学公共卫生学院吴婷教授介绍,今年4月底在美国华盛顿召开的2023年第35届国际乳头瘤病毒大会(IPVC)上,非营利国际健康科技组织PATH报告了其发起的厦门万泰二价HPV疫苗馨可宁®与美国默沙东公司四价HPV疫苗佳达修(Gardasil)的头对头研究试验期中分析结果。据悉,该研究在加纳和孟加拉国开展,入组1025名9-14岁女性志愿者,结果显示馨可宁®具有良好的免疫原性,9-14岁女性在接种1针馨可宁®6个月后,其HPV16和HPV18的IgG抗体滴度、阳转率均高于佳达修。
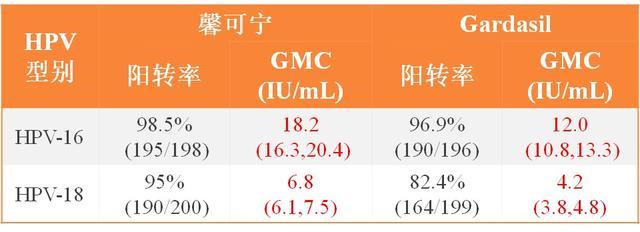
安全性方面,在“征集性局部不良反应”、“征集性全身不良反应”、“非征集性不良事件”三项指标的评估中,馨可宁®与佳达修表现相近,馨可宁®的不良反应发生率不高于佳达修。
2022年,国际顶级医学期刊《柳叶刀-感染病学》发表的一项5.5年随访结果显示,馨可宁®在预防18-45岁女性人群HPV16/18的相关癌前病变终点的保护率达到100%,并可诱导高水平抗体,具有良好免疫持久性和极高的安全性。
目前市面上的HPV疫苗主要有5款,其中3款为进口疫苗,分别为美国默沙东公司的四价疫苗(佳达修4)、九价疫苗(佳达修9),以及英国药企葛兰素史克的二价疫苗希瑞适(CervarixT),2款为国产疫苗,分别为厦门万泰的二价疫苗馨可宁®和沃森生物的二价疫苗沃泽惠。
疫苗的价次是指疫苗所能预防的病毒亚型数量,二价HPV疫苗可预防HPV16、18型,四价HPV疫苗可预防HPV6、11、16、18型,九价HPV疫苗可预防HPV6、11、16、18、31、33、45、52、58型。
2022年5月,医学期刊《疫苗》(Vaccine)上的一项研究从政府和社会角度评估了四种不同宫颈癌疫苗产品——馨可宁®、希瑞适、佳达修®佳达修9用于10组9岁女童常规HPV疫苗接种的潜在成本效益,结果显示,与从未接种过HPV疫苗的人群相比,馨可宁®最具成本效益。
厦门万泰技术副总经理潘晖榕介绍,目前生产HPV疫苗的技术路线主要有三种:昆虫细胞、酵母细胞和大肠杆菌。馨可宁®所采用的技术路线是由厦门大学与厦门万泰团队自主创新的大肠杆菌病毒样颗粒技术平台,其优势在于大肠杆菌是原核生物,其生长速度快,生产周期短,产量高。而且大肠杆菌是人体正常菌群,免疫排斥低,安全性高。
接种疫苗不要等待
据厦门万泰介绍,从研发到获批上市,馨可宁®共经历了16年历程。其抗原表达技术路线探索从2002年就开始了,2010年馨可宁®获批Ⅰ期临床试验,到2019年获批上市,历时多年。
国产九价HPV疫苗的上市还有多远?据悉,IPVC大会上同期公布了厦门万泰的九价HPV疫苗(馨可宁®9)和佳达修9在18-26岁女性中的头对头免疫原性比较结果。数据显示,馨可宁®9的免疫原性、耐受性均表现良好,9种抗体中有5种型别中和抗体几何平均浓度点值略高于佳达修9,4种型别中和抗体几何平均浓度点值略低于佳达修9,总体效果相当。
吴婷表示,目前馨可宁®9正在临床试验中,希望能够在今年年底积累到足够的病例数,在明年年终前提交数据。潘晖榕补充,除了临床试验的数据,厂房的建设和工艺的开发也要达到标准,这两方面的工作都完成后,他们会向国家药品监督管理局提交上市申请,国家药品监督管理局会对资料进行审核。产品上市前,还需要进行生产现场核查,即药监局到工厂现场查看产品的制造,并抽样送到中国食品药品检定研究院进行检测,产品必须检测合格。“这是一个很复杂的过程,我们希望加快九价HPV疫苗的生产进程,但是影响因素很多,因此存在一定的不确定性。”
接种二价还是等待九价?这是让很多人犹豫不决的问题。近期21世纪经济报道、21世纪新健康研究院发布的一项《HPV疫苗消费行为调研》结果显示,在中国,适龄女性对于HPV疫苗的接种意愿高;但受限于疫苗应用价值的认知偏差,以及部分适龄女性在疫苗选择时会执着“价数”形成“疫苗犹豫”、等待等状况,影响了实际接种率。
在2021年2月发布的《人乳头瘤病毒疫苗临床应用中国专家共识》中,包括北京大学人民医院妇产科主任魏丽惠等在内多位专家呼吁尽早接种HPV疫苗,“低龄人群接种效果优于高龄人群,性暴露前接种免疫效果最佳”。
2022年8月底,默沙东宣布其九价HPV疫苗适用人群扩展至9-45岁女性。澎湃科技记者曾连线复旦大学附属肿瘤医院妇瘤科副主任、主任医师温灏解读,温灏表示,宫颈癌疫苗的“价”数越高,表明覆盖的HPV亚型越多,对机体的保护作用也越强。最佳接种年龄是首次发生性生活之前。一般而言,年纪越轻机体免疫力越强,疫苗接种后产生的抗体的保护作用越强,持续时间也会越长。因此建议在条件允许的情况下应尽早接种。(详见澎湃科技报道:《HPV疫苗新适应证获批,专家:9-45岁女性应接尽接》)
