1类新药获批上市:莫博赛替尼为非小细胞肺癌患者提供了新的治疗选择
转自:药事纵横
2023年1月11日,国家药品监督管理局通过优先审评审批程序附条件批准武田制药公司申报的1类创新药琥珀酸莫博赛替尼胶囊(商品名:安卫力/EXKIVITY)上市。该药适用于含铂化疗期间或之后进展且携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者[1]。
莫博赛替尼是一种靶向EGFR第20外显子插入突变的不可逆的酪氨酸激酶抑制剂。该药品的上市为携带EGFR外显子20插入突变阳性的晚期非小细胞肺癌患者提供了新的治疗选择。
EGFRex20ins分子结构及耐药机制
表皮生长因子受体20 号外显子插入突变(epidermalgrowthfactorreceptorexon20insertions,EGFRex20ins)是非小细胞肺癌(non-smallcelllungcancer,NSCLC)中的一种罕见突变,约占NSCLC患者1%~2%,占所有EGFR突变NSCLC患者4%~10%[2]。EGFRex20ins包含两个重要区域:调节C-螺旋结构域(AA762-766)及C-螺旋后的邻近环(AA767-774)。
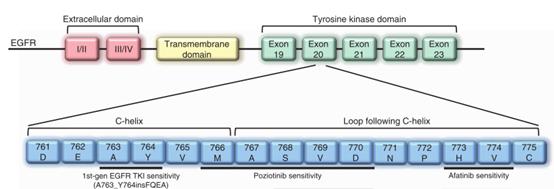
EGFR突变型NSCLC中的外显子20插入AA761和AA775之间的3-21个碱基对的框架内并通过将C螺旋推入其内部位置以配体无关的方式激活受体,诱导活性受体构象。基于表皮生长因子受体(EGFR) 酪氨酸激酶抑制剂(TKI) 的靶向治疗是携带EGFR突变型晚期非小细胞肺癌(NSCLC) 患者的一线靶向治疗,由于EGFRex20ins结构的特异性,传统的TKI治疗并不适用于该类患者,当C-螺旋进入激活状态后,C-螺旋及磷酸结合环被推入药物结合口袋中,这一立体位阻效应阻碍了EGFR与TKI的结合,从而产生耐药[3]。
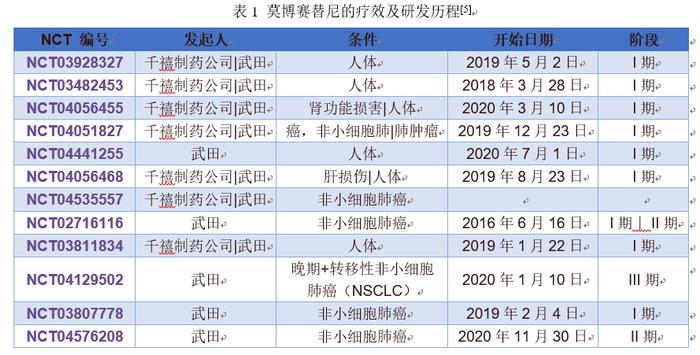
莫博赛替尼的疗效及研发历程
莫博塞替尼是一种与EGFR中的半胱氨酸797共价结合的EGFR和HER2TKI,其独特之处在于可识别并靶向αC-螺旋附近蛋白质之间的细微结构差别并产生不可逆结合,在临床前Ba/F3模型中显示,与其他TKI相比,它在抑制EGFRins20方面具有更好的选择性。同时,莫博塞替尼及其两种活性代谢物AP32960和AP32914在抑制EGFR方面几乎同样有效。
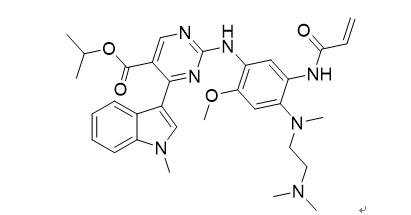
Mobocertinib结构式
CAS号:1847461-43-1
一项开放标签、多中心I/II期临床研究(NCT02716116)[4]采用扩大队列来评估Mobocertinib在转移性EGFRex20ins突变的NSCLC患者中的安全性、耐受性和抗肿瘤活性。Mobocertinib是一种针对EGFRex20ins突变的EGFRTKI,在EGFRex20ins阳性的NSCLC患者的RP2D为160mg/d时显示出抗肿瘤活性,确诊的ORR为43%,中位反应持续时间为14个月,中位PFS为7个月。Mobocertinib的AE曲线是可管理的,并与其他EGFRTKIs的AE曲线一致。
与poziotinib类似,最常见的副作用是胃肠道,160毫克治疗的患者中92%有任何级别的腹泻(16%级别≥3),28%有恶心。45%出现皮疹。 治疗相关的不良事件导致21%的患者剂量减少,10%的患者停止治疗。
2021年5月24日,国家药品监督管理局药品审评中心(CenterforDrugEvaluation,CDE)发布公示将Mobocertinib纳入优先审评审批。7月,MobocertinibⅠ/Ⅱ期试验的结果已获CDE受理并正在审评中。2023年1月11日获NMPA附条件批准上市。
基于这些初步结果,FDA批准了莫博塞替尼孤儿药物指定(2019),随后批准了突破性治疗指定(2020年4月)。这是2020年批准的两项突破性治疗方案之一,用于以前治疗过的晚期EGFRex20ins非小细胞肺癌,对于当时没有任何批准的靶向治疗的肿瘤类型来说,这是一项重大的临床进展。
其他治疗药物
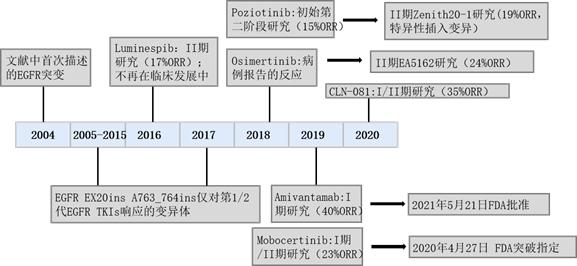
过去的5到10年中,针对这一独特的分子亚群已经开发了许多紧急疗法和临床试验,这些新的治疗方法具有多种作用机制和不同的临床活性水平,在改善EGFRins20突变患者的治疗选择方面迈出了重要的一步[2]。其中包括Poziotinib(15%ORR)、Osimertinib(24%)、Tarloxotinib(0%)、Luminespib(17%)等等。
总结
尽管自EGFRTKIs的发展以来,NSCLC中典型的、致敏的EGFR突变患者的临床结果有了显著的改善,但携带EGFRins20的肿瘤患者尚未看到突破性的临床进展。历史性的挑战包括诊断方法的局限性(因为一些早期的基因分型分析缺乏EGFRins20检测的覆盖面),存在的不同ins20变异体的数量,以及用于实验室研究的临床前模型的相对缺乏。
这些障碍最初限制了进展,延迟了我们对携带EGFRins20的NSCLC肿瘤的频率和生物学特征进行可靠量化的能力。随着测序技术的快速改进和临床资料的仔细回顾,在过去的十年中,EGFRins20作为EGFR突变型NSCLC的第三个最常见亚型得到了更清楚的认识,它具有独特的生物学特性,需要有自己的专用方法来开发靶向治疗。莫博赛替尼在中国的获批上市为中国非小细胞肺癌患者带来新的治疗选择,填补了临床治疗的空白。
参考资料与文献
[1]NMPA官网:国家药监局附条件批准琥珀酸莫博赛替尼胶囊上市(nmpa.gov.cn)
[2]CatherineB.Meador,LeciaV.Sequist,ZofiaPiotrowska;TargetingEGFRExon20InsertionsinNon–SmallCellLungCancer:RecentAdvancesandClinicalUpdates.CancerDiscov1September2021;11(9):2145–2157.
[3]郑彩云, 高晨杨, 施恩,等. 非小细胞肺癌EGFR20号外显子插入突变的药物研究进展[J]. 临床合理用药杂志 2021年14卷10期,178-181页,2021:福州市科技计划项目.
[4]RielyGJ,NealJW,CamidgeDR,SpiraAI,PiotrowskaZ,CostaDB,etal.Activityandsafetyofmobocertinib(TAK-788)inpreviouslytreatednon-smallcelllungcancerwithEGFRexon20insertionmutationsfromaphase 1/2trial.CancerDiscov2021.
[5]MCE官网:https://www.medchemexpress.cn/mobocertinib.html
