癌症相关恶病质—了解肿瘤的宏观环境和微环境以改善治疗
转自:药时空
背景:恶病质是一种毁灭性的、多因素的、通常不可逆的全身性综合征,其特征是体重显著下降(主要是骨骼肌和脂肪组织),发生于约50-80%的癌症患者。虽然恶病质主要累及骨骼肌(约占体重的40%),但恶病质是一种多器官综合征,也涉及白色和棕色脂肪组织,以及骨骼、脑、肝、肠和心脏等器官。值得注意的是,恶病质占癌症相关死亡的20%。癌症相关恶病质总是与全身炎症、厌食和能量消耗增加相关。了解这些机制至关重要,过去10年在这一领域取得的进展有助于开发新的治疗方法。
简介:
2023年2月20日,来自西班牙巴塞罗那大学生物学院生物分子学系的JosepM.Argilés教授课题组在NatRevClinOncol(IF:65.0)杂志上发表题为“Cancer-associatedcachexia-understandingthetumourmacroenvironmentandmicroenvironmenttoimprovemanagement”的文章[1]。在这篇综述中,作者分析了目前关于肿瘤宏观环境和微环境在癌症相关恶病质中的作用的证据,并提供了一种新的治疗策略来管理这一综合征的概述。

主要结果:
系统性生物学改变。
癌症相关恶病质是癌细胞、TME细胞和其他细胞类型促进的全身性炎症的结果,影响许多组织和器官,是该病的许多全身性症状的基础,如肌肉无力、心脏功能改变(包括心率加快和心脏萎缩)、肠道吸收不良、味觉和嗅觉改变、在一个由约2,600名癌症相关恶病质患者组成的队列中,随着时间的推移,中性粒细胞与淋巴细胞比值(全身性炎症的标志)的增加与较差的OS相关(HR1.51,95%CI1.33~1.71)。在癌症患者中,恶病质还与骨和骨骼肌的丢失相关,而骨骼肌实际上可以调节骨量,因此强调了这两种组织之间的相互作用。这种相互作用由组织释放的细胞因子(肌因子和骨因子)介导。此外,肝功能的变化(如结构蛋白合成减少和分泌蛋白合成增加)会导致急性时相反应,导致CRP生成和释放增加,而白蛋白释放减少,从而降低白蛋白/CRP比值(炎症的重要标志物)。
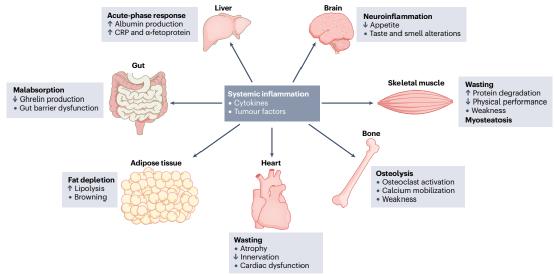
TME的生物学改变。
癌症相关恶病质的相关因素。
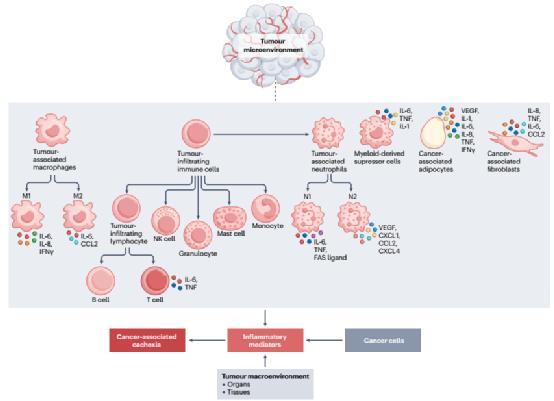
对引发癌症相关恶病质代谢改变的分子机制的研究发现了大量介导这些效应的介质,这些介质可以由非恶性细胞(主要是免疫细胞)和/或癌细胞分泌。临床前模型中描述的关键介质包括IL-6、TNF、IL-1β、基质金属蛋白酶9、脂质运载蛋白2和GDF15。此外,与良性胰腺疾病患者相比,晚期胰腺癌患者血清中GDF15水平升高。遗憾的是,阻断上述分子的临床前和临床策略通常未能改善对肌肉质量和功能的保护。
肿瘤分泌的细胞外囊泡。
许多蛋白质、代谢物、脂质和微小RNAs(miRNAs)包裹在不同大小的细胞外囊泡中在血液中循环,包括直径为30~150nm的外泌体和100~1000nm的微囊泡。细胞外囊泡在多种生理病理过程中参与细胞间和器官间的通讯,包括癌症和癌症相关恶病质。事实上,临床前研究表明,肿瘤可分泌携带CIFs的细胞外囊泡。例如,在小鼠模型中,肿瘤分泌含有热休克蛋白70(HSP70)和HSP90的细胞外囊泡,这些囊泡通过激活toll样受体4(TLR4)信号通路导致肌肉消耗。
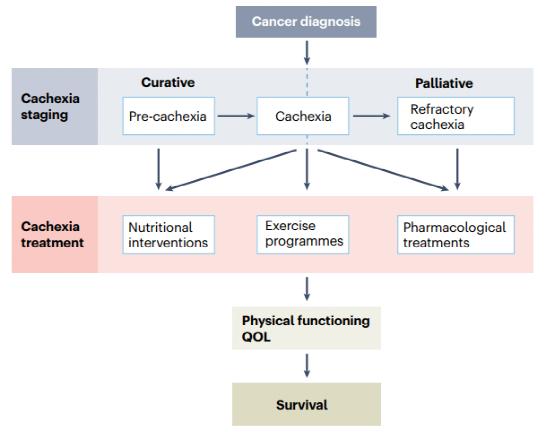
将生物学转化为疗法。
尽管针对癌症相关恶病质开展了大量研究,并取得了有希望的结果,但这些发现尚未转化为有效的治疗方法,因此遗憾的是,目前尚无针对这类患者的标准治疗。然而,ESMO和欧洲临床营养与代谢学会(EuropeanSocietyforClinicalNutritionandMetabolism)等几个组织已经制定了临床指南。迄今为止,对这些患者的管理包括营养建议或补充,对严重影响的患者进行药物治疗,包括孕激素、醋酸甲地孕酮和/或皮质类固醇。目前的国际指南强烈建议通过营养、物理和药理方法促进合成代谢和减少分解代谢。事实上,在过去的几年里,营养咨询和药物补充剂的结合已经成为一种多模式的方法,比依赖单一的药物或“灵丹妙药”更有效。“此外,癌症相关的恶病质患者需要适当的体育锻炼计划,这可以提高生活质量,也可以有有益的抗炎作用。
药物治疗。
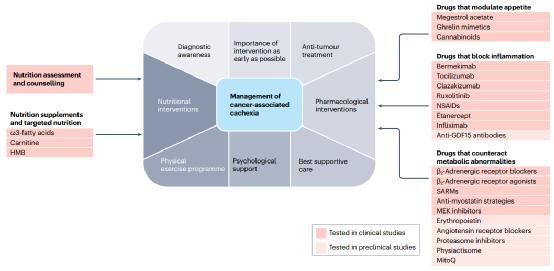
了解癌症相关恶病质的营养和代谢改变,并识别这些改变涉及的通路,有助于制定药理学策略。这些策略包括刺激食物摄入、减少炎症和缓解代谢异常。
与抗癌疗法的相互作用。
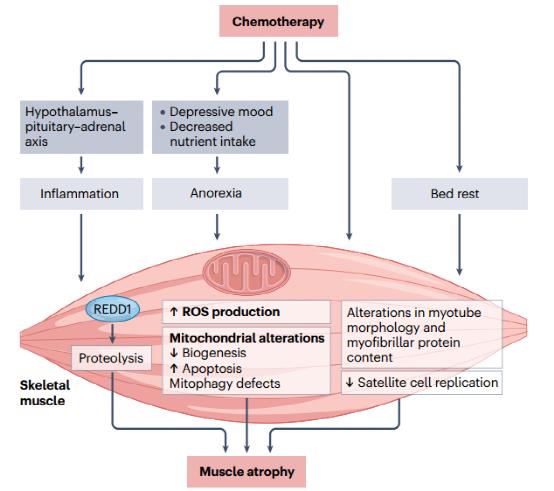
化疗通过与进食相关的不良反应(包括恶心和呕吐)影响营养;因此,这些治疗方式可能导致厌食和肌肉消耗,从而导致体重减轻。此外,大多数化疗药物可诱导肌病反应,涉及骨骼肌萎缩和功能障碍。事实上,这些药物刺激中枢神经系统的下丘脑-垂体-肾上腺轴,导致糖皮质激素释放和促炎细胞因子(包括IL-1α、IL-1β、IL-6和TNF)的产生。化疗的许多不良反应可影响中枢神经系统,包括脑病综合征和精神错乱状态、癫痫发作、头痛、脑血管并发症、视力丧失、小脑综合征和脊髓病。最常引起中枢神经系统毒性(表现为不同程度脑病)的化疗药物包括甲氨蝶呤、长春新碱、异环磷酰胺、环孢素、氟达拉滨、阿糖胞苷、5-氟尿嘧啶、顺铂和干扰素。此外,将培养的成肌细胞暴露于卡铂可增加REDD1的转录,导致骨骼肌萎缩。在机制上,该基因的产物激活NF-κB和MAPK信号通路,通过激活泛素-蛋白酶体系统刺激萎缩反应。在小鼠癌症模型中,接受化疗也会导致运动单位连接丧失,从而影响突触前形态,并导致肌肉神经支配发生改变。
在培养的大鼠骨骼肌细胞中,化疗药物影响肌管形态、肌原纤维蛋白含量和底物利用率(图5)。一些化疗药物还通过促进高水平ROS的产生,在培养的成肌细胞中诱导线粒体功能障碍,因此表明应激敏感的信号介质(ROS和反应性氮物质)可能作为与恶病质相关的化疗诱导肌病的共同信号通路。此外,线粒体功能障碍(在激活肌肉萎缩中起关键作用)的发生似乎与ROS产生过多相关。对接受新辅助化疗的早期乳腺癌患者骨骼肌组织的分析显示,线粒体生物发生减少,伴有线粒体动力学改变、线粒体自噬缺陷和凋亡激活。
除了对分化的骨骼肌有有害影响外,化疗药物还影响卫星细胞的复制,从而影响肌肉的生长和修复(图5)。在细胞培养模型中,化疗药物破坏了肌小节组织,导致骨骼肌细胞的收缩能力发生改变。在该模型中,化疗诱发的肌小节紊乱损害了组蛋白修饰酶的活性,导致分子马达蛋白肌球蛋白重链ⅱ丢失。
建立恶病质指数(CXI)是为了评估化疗对癌症相关恶病质的效果。CXI计算综合了第3腰椎水平的骨骼肌指数、血清白蛋白水平和中性粒细胞与淋巴细胞比值。CXI临界值取决于肿瘤分期,并根据时间依赖性受试者工作特征曲线确定。在小细胞肺癌或弥漫性大B细胞淋巴瘤和恶病质患者中,低CXI与治疗不耐受(不良事件发生率增加)和低客观缓解率相关。因此,CXI是一个很有前景的生物标志物,可以指导癌症相关恶病质患者的化疗,而需要在其他肿瘤类型的患者中进行检测。
结论和展望:
与许多其他疾病的情况相似,临床前模型提供了可以外推到人类的癌症相关恶病质的分子机制。癌症的临床前模型有局限性,包括与人类肿瘤相比,肿瘤生长更快,以及在某些情况下,由于解剖位置不正确和TME的差异,非原位接种可能无法真实地再现肿瘤行为。遗憾的是,尽管在过去的15年中,我们对癌症相关恶病质的生物学和分子基础的理解有了长足的进步,但有效的生物标志物(尤其是血液或尿液中的标志物)却很少。癌症相关恶病质的有效早期检测尚未得到满足,因为发生于许多癌症患者的晚期恶病质通常难以治疗。另一个未满足的需求是深入了解癌症相关恶病质的分子途径,以便设计有效的治疗策略,治愈或至少改善这种疾病。目前,肿瘤科医师基本上使用的是几十年前建立的治疗方法(如醋酸甲地孕酮或糖皮质激素),这些治疗方法长期无效。这些治疗应该被考虑到所获得的分子知识的新方法所取代。
为了改善恶病质的治疗,有三个考虑因素很重要:首先,鉴于恶病质是一种多器官和多因素综合征,单一药物不太可能提供满意的结局,需要多模式方法。这种方法应综合营养咨询和补充、运动干预和药物干预(特别考虑ghrelin类似物和β受体激动剂)。其次,由于肿瘤对氨基酸的需求非常高,因此治疗策略不仅应侧重于阻断分解代谢(抑制肌肉蛋白水解和防止脂质流失),还应侧重于合成代谢(即蛋白质合成)。第三,任何成功的治疗应该在癌症确诊后尽快开始,应该是多学科的,应该包括综合征的分期。在提供符合当前临床指南的治疗时,后一个方面是绝对必要的。
参考文献:
[1]ArgilésJM,López-SorianoFJ,StemmlerB,BusquetsS.Cancer-associatedcachexia-understandingthetumourmacroenvironmentandmicroenvironmenttoimprovemanagement.NatRevClinOncol.2023Feb20.doi:10.1038/s41571-023-00734-5.Epubaheadofprint.PMID:36806788.
