重磅ADC「德曲妥珠单抗」胃癌适应症拟纳入优先审评
转自:医药观澜
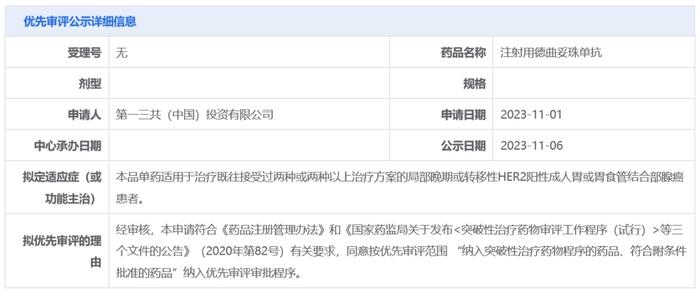
11月6日,中国国家药监局药品审评中心(CDE)官网公示,第一三共(DaiichiSankyo)申请的注射用德曲妥珠单抗新适应症拟纳入优先审评,单药适用于治疗既往接受过两种或两种以上治疗方案的局部晚期或转移性HER2阳性成人胃或胃食管结合部腺癌患者。公开资料显示,德曲妥珠单抗(Enhertu)是阿斯利康(AstraZeneca)和第一三共联合开发的一款靶向HER2的抗体偶联药物(ADC),此前已在中国获批治疗HER2阳性和HER2低表达成人乳腺癌患者。
胃癌是全球常见癌症,也是癌症死亡重要原因之一。腺癌是胃癌的主要组织学亚型,大约占全球报告病例的90%以上。据统计,大多数中国胃癌患者在确诊时已经处于晚期,治疗选择有限。大约五分之一的胃癌是HER2阳性。HER2是一种酪氨酸激酶受体,它表达在许多肿瘤类型中,包括乳腺癌、胃癌和结直肠癌。
德曲妥珠单抗由靶向HER2的人源化单克隆抗体通过四肽可裂解连接子与拓扑异构酶1抑制剂有效载荷连接组成。该药的作用机理为:首先通过药物中的抗体部分靶向并附着于癌细胞上的HER2;然后德曲妥珠单抗会进入癌细胞,释放化疗药物,ADC中的化疗部分可以杀死癌细胞以及附近的其它细胞。
2023年2月,德曲妥珠单抗在中国获批治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者;同年7月,该产品新适应症再获批准,单药适用于既往在转移性疾病阶段接受过至少一种系统治疗的或在辅助化疗期间或完成辅助化疗之后6个月内复发的,不可切除或转移性HER2低表达成人乳腺癌患者。根据CDE公示,此次德曲妥珠单抗拟纳入优先审评,针对适应症为HER2阳性成人胃或胃食管结合部腺癌。

此前,德曲妥珠单抗已在一项治疗HER2阳性局部晚期或转移性胃癌和胃食管结合部腺癌患者的随机2期DESTINY-Gastric01试验中取得积极结果。数据显示,与接受化疗的患者相比,接受该产品治疗的患者客观缓解率(51.3%vs14.3%)和总生存期(中位OS:12.5个月vs8.4个月)获得显著改善。在预先指定的中期分析中,接受德曲妥珠单抗治疗的患者与接受化疗的患者相比,死亡风险降低了41%。基于该研究结果,该产品已获得FDA批准扩展适用范围,用于治疗HER2阳性局部晚期或转移性胃癌和胃食管结合部腺癌患者。
在另一项针对西方胃癌患者进行的代号为DESTINY-Gastric02的2期临床试验中,德曲妥珠单抗治疗HER2阳性转移性或不可切除胃癌或胃食管连接部腺癌也取得了积极疗效结果。试验主要分析显示,德曲妥珠单抗达到38%的总缓解率(ORR),其中包括3.8%的完全缓解(CR)和34.2%的部分缓解(PR)。在中位随访时间为5.7个月时,中位缓解持续时间为8.1个月,无进展生存期为5.5个月。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.RetrievedNov6,2023,fromhttps://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731
[2]Enhertulabel.RetrievedJan15,2021,fromhttps://www.accessdata.fda.gov/drugsatfda_docs/label/2021/761139s011lbl.pdf
[3]EnhertuII期临床试验DESTINY-Gastric02彰显其对HER2阳性晚期胃癌患者的临床意义和持久应答反应.RetrievedSep20,2021,fromhttps://mp.weixin.qq.com/s/0L_gMLFmSmuHvGsjGsSmhg
