生物分析专栏 | 中药的药代动力学及其生物分析
转自:阳光诺和
01
前言
中药是指在中医理论指导下,用于预防、治疗、诊断疾病并具有康复与保健作用的物质。中药主要来源于天然药及其加工品,包括药材和饮片、植物油脂和提取物、成方制剂和单味制剂。《中华人民共和国药典(2020年版)》一部中收载中药2711种[1]。中药是中国人民上千年用药实践的总结,是世界医学的瑰宝。西药通常化学成分单一,靶点明确,作用机制明确,而中药通常为多组分、多途径、多靶点相互作用,协同发挥药效。尤其,中药对于慢性病的治疗上具有独特的优势。
中药药代动力学(PharmacokineitcsofTraditionalChinesemedicine)是借助于动力学原理,研究中药活性成分、组分、中药单方和复方在体内的吸收(absorption,A)、分布(distribution,D)、代谢(metabolism,M)和排泄(excretion,E)(简称ADME)的动态变化规律及其体内时量-时效关系,并用数学函数加以定量描述的一门学科[2],它是中药药理学的重要分支,对阐明中药药效物质基础、揭示中药有效性与安全性的科学内涵、中药新药研发与剂型改进及方剂配伍机制、以及优化中药临床治疗、指导临床合理用药等方面均发挥了十分重要的作用[3]。
中药常以复方入药,其含有的几百上千种成分同时进入人体,有效成分复杂、多变,使得其在体内的ADME特征以及动力学特征与西药经典药代动力学具有很大的差异。如何科学评价中药在机体内的药代动力学特征、体现中药药代动力学对整体性特点、揭示中药药效作用物质基础、阐明体内暴露量与药效的相关性意义重大。本文将从中药的特点、中药的药代动力学特点、中药药代动力学的研究思路与方法、中药药物相互作用研究、中药的生物分析方法几个方面进行论述。
02
中药的特点
中药新药研究大多是在已有临床应用经验和确切疗效的中药方剂基础上的研究,其“源于临床-证于实验-回归临床”的研究过程体现了中药研究的特点和规律[4]。
(1)中药制剂具有多成分、多靶点、多效应的特点。中药制剂采用源于自然界的植物、动物和矿物为原料,又具有四气五味、升降沉浮等药性特点,常以复方入药。用药时需遵循君臣佐使、七情和合、去性存用、升降相因、五行配伍等配伍理论。因此中药通常是由多种成分组成的复杂体系,由多种化学成分相互作用多靶点发挥多效应的药效作用。比如,心血管疾病、癌症、精神疾病等涉及多种分子机制的失调,而非单一机制的失调。应对这些复杂疾病,复方药物和联合用药常常具有治疗优势[5],这也体现了中药的整体作用的特点。
(2)中药的有效成分的含量存在差异。中药由于其“道地药材”的属性使得其不同产地的药材有效成分的含量存在差异,从而会带来药效上的差异。另外,中药通常经过蒸、煮、炒、炙等工序加工炮制入药。中药材经炮制后,其主要成分也可能发生质和量的变化。比如,从疗效角度来讲,有毒中药通过炮制可以达到增效减毒、缓和药性的目的。
(3)传统中药大都是口服给药,胃肠道的pH环境变化会影响药物的吸收[6]。
中药的特点也是其研究的难点。比如:中药成分复杂,如何选择药效指标代表药物对机体作用的整体性?同时,中药复方具有多味药物组成,复方中的药物之间、化合物和化合物的作用纷繁复杂,从而会导致药代动力特征不同寻常,如何解读这些特征以及药代-药效的相关性?
03
中药的药代动力学特点
中药药代动力学研究内容包括考察给药后中药的体内物质暴露;研究中药活性成分的药动学特征、吸收和体内变化过程(分布、代谢、排泄)以及相关的分子作用机制;研究中药成分体内暴露和药代特征与其药效作用的关系;考察与其成分体内暴露和变化过程关联的中药安全性问题;研究方剂配伍的药代机理和作用模式、中药与化药合用时的药代问题等[5]。
中药的药代动力学的研究过程不同于化药,化药的药代动力学研究是从药物的发现到临床研究阶段,可为药物候选物的成药性评价提供支持;而中药的药代动力学研究是从临床实践回到科研再走向临床实践的过程。中药的药代动力学的研究可为中医药理论提供依据。
中药提取物、中药配伍、中药炮制均呈现具中药特色的药代动力学特点。中药活性单体与提取物的药动学比较研究,发现提取物中的共存成分对活性标识成分体内过程的影响较为复杂。其影响可能是促进吸收、增加暴露程度、延长滞留时间;也可能是抑制吸收,降低暴露程度,缩短滞留时间;甚至同一结构类型的不同成分也可能表现出不同的变化趋势[7]。配伍是复方中药的核心理论,药对配伍的目的是增效减毒,不同的配伍比例和配伍药味会影响药物中有效成分在体内吸收代谢过程:配伍后可能使药效成分在体内吸收增加、暴露量增加、滞留时间延长,起到增效的作用[8,9];同时,也可以降低毒性成分在体内的吸收和暴露、缩短滞留时间,起到缓和药性、减毒的作用[10,11]。有些药对配伍后对不同成分具有不同甚至相反的药动学影响[12,13]。中药提取物通过炮制过程溶出有效成分,可促进有效成分的吸收以及调控CYP450酶的作用可增加部分活性成分的生物利用度,同时,可降低无关成分的生物利用度[14-16]。此外,有研究表明,醋炙在一定程度上提高了活性成分的肝脏靶向效果,为醋主入肝经、醋炙可缓和药性的炮制作用提供了理论依据[17]。上述研究为中药的炮制理论提供了现代药动学数据的支持[18-20]。
口服给药方式为传统中药的服用方式,中药进入人体后,必然会接触肠道菌群。中药可通过肠道菌还原、水解转化为有效成分发挥药效。王琰、杨秀伟等国内专家学者在生物碱、黄酮、多糖、皂苷等中药成分与肠道菌的相互作用研究方面积累了大量的数据,为中药肠道菌代谢研究提供了科学依据[21,22]。
此外,中药的人体药代动力学在中药新药的研究中至关重要。但由于伦理学等方面的限制,很难直接在人体上开展研究[3]。并且面临诸多难题,如复方中药新药的剂量与疗效之间很难找到明显的量效关系,这或许与中药成分多种多样,使得药物与疗效之间未必存在线性关系有关[23,24]。
04
中药药代动力学的研究思路与方法
以1963年陈琼华教授对大黄的药代动力学研究为代表,80年代国内外学者对中药的有效成分和单味中药进行药代动力学研究,到了90年代,开始着重对对中药复方及中成药进行研究。这些方法均是尝试用中药或复方中药效作用明确的某一个或某几个成分来代表中药整体进行研究,这对某些中药药代动力学研究起到了一定的作用[25]。但是,中药的药效是多种化学成分相互作用、中药与机体相互作用所产生的综合结果,单纯采用西方植物药研究方法无法阐明中医药的科学内涵。中药多组分药代动力学仍是以寻找中药及复方中的活性物质为研究重点,与以往研究的不同之处在于,该类研究充分考虑了中药“整体观”的特点和中药有效成分在体内的变化过程,综合运用多学科知识和现代先进的分离分析手段,构建中药及其复方吸收、分布、与靶细胞结合的体内外技术平台,通过寻找中药发挥作用的体内效应成分(群),来追溯其在中药直接提取物中的物质形式[25]。基于组学的中药药代动力学研究从机体对中药产生的内源性小分子应答这一角度,通过同时监测中药原型及被代谢成分(药代)和内源性小分子代谢物(代谢组)的变化,探索中药与人体两个系统之间的相互作用[26]。具有中医药特色的中药的药代动力学-药效动力学(PK/PD)结合的研究方法着眼于药物的体内过程、药物效应及二者之间的关系,有利于阐明药物作用机制,且以现代科学阐述中药组方原理,为研究古方、筛选新方提供科学依据和方法[25]。
1、中药多组分药代动力学
传统中药物质基础研究思路和方法来源于西方天然药物的研究思路,即对中药的化学成分进行提取、分离、结构鉴定,然后评价生物活性,确定有效成分[27]。中药的疗效通常来源于复方中多种药效物质的综合作用,而经纯化分离后,中药的内在系统联系亦被割裂,中药多组分、多靶点、多途径的协同作用机制无法展现,也就难以反映其整体辨证施治的优势所在[26]。
考虑到中药组分协同用药的整体思想,许多学者采用同时定量描述多个单体成分的动力学,以此来描述中药整体的动力学特征[28]。选择中药药代标识物开展多组分药代动力学研究有助于阐明主要活性成分在体内的药代特征,是中药物质基础研究的重要内容。中药药代标识物指以给药后体内出现的并能用现有分析技术检测的中药物质(原型成分或代谢物),来反映或预测与中药药效或安全性关联的中药体内物质暴露、影响暴露的因素及与暴露相关的其他重要因素[5]。
活性单体与中药提取物药代动力学比较研究可通过分别测定多种单体和(或)单体混合以及相当剂量的中药提取物给药后各成分的药动学参数,比较其差异来分析中药提取物多成分药动学相互作用。中药提取物药对配伍的药代动力学研究则可通过比较单味提取物与药对混合提取物在分别给药后的体内药动学参数的差异,分析存在的药动学相互作用,阐述可能的配伍机制。炮制的中药多组分药代动力学可通过对比中药炮制前后人血成分药动学参数的差异阐明炮制的内在作用机制[7]。
由于中药化学成分的复杂性和多样性,以及机体状态的不可预测性,给治疗的物质基础研究带来许多问题[2],屠鹏飞等[27]综述了中药物质基础研究的方法。
还有学者提出基于权重的多效应成分分类整合药代动力学研究的概念,即针对效应成分相对明确的复方中药,按化合物类型对由中药复方所含多种有效成分分类成可数的类群,对分类整合后总类群的经时变化血药浓度,用经典的药代动力学理论与模型进行描述的方法。但是,由于复方中药成分复杂,部分明确的有效成分能否代表该复方中药并不确定,基于权重的药代动力学分析更增加了药代动力学参数的不确定性,该方法无法指导药物的用法用量,也无法进行治疗药物的监测[29]。
中药成分众多,尤其经组方配伍后的中药复方化学成分更加复杂,使得各成分的药代特征相差较大。单体成分的药动学参数简单叠加并不能代替整体药动学效应,虽能体现单体间的相互作用,但无法反映中药的整体性[26]。同时,某些微量甚至痕量成分,以及药物等代谢产物表现为血药浓度低,难于检测或富集,无法评估其活性。上述诸多因素,导致多组分药代动力学无法指导中药的临床用药。
2、基于组学的中药药代动力学研究
多组分药代动力学研究不足以反映中药的整体性特征,有学者提出了基于组学的研究思路,包括化学物质组学、中药药代动力学-代谢组学。罗国安等[30]认为中药复方和人体之间是一个“干预-应答”相互作用的生物学过程,而这种应答可以用代谢组学来准确表征。代谢组学可以间接地反映中药复方的药代动力学的特征,甚至能反映药动学个体差异。
化学物质组学是将单味中药或中药方剂所含的复杂成分看作组合化学库或化学物质组,采用组合化学或组学的方法研究中药物质基础[31],即将中药进行分离后,采用现代仪器分析方法如液质联用技术、高分辨质谱等对各成分进行解析,再确定活性物质组[27]。
代谢组学是对生物体体液、组织中的内源性和外源性小分子代谢产物(小于1500Da)进行靶向和非靶向的定性、定量分析。通过代谢组学分析患者和健康生物样本的代谢谱差异,可以发现与疾病密切相关的特异性生物标志物,为疾病的病理变化机制提供重要的参考。中药代谢组学是研究给予中药后,药物对机体代谢通路的影响。中药代谢组学可以动态监测给药后动物体代谢谱图的变化趋势,可用于发现与毒物相关的生物标志物,在中药毒理学研究中发挥越来越重要的作用。中药药效代谢组学研究也存在着成分不清、科学问题不明确、缺乏深入的靶点探索等问题[32]。
中药药代动力学-代谢组学的研究是基于代谢组学的研究方法研究中药和机体的相互作用,以期阐明药代-药效相关性。根据中医“症候”理论,以药效为基础,逆向解析中药进入体内后所导致的与机体生理、病理状态息息相关的内源性小分子代谢物变化与药物经时变化的相关性,进而阐明药物的代谢通路和作用机制,以及中药副作用产生机制等问题。该方法从现代药理学的角度揭示中药的作用机制,提示中药发挥作用的可能代谢途径,甚至可能发挥作用的靶点通路。这种自下而上的研究模式有利于克服当前中药药动学和中药代谢组学研究中的种种不利因素,牢牢把握疾病-人体-中药三者之间的因果关系,符合中医药整体观的研究方法论,使得对中药复杂体系的药效物质基础的研究有的放矢,为中药功效物质基础的研究以及中医辨证论治理论研究开辟了局面。
此外,如何将生物体内代谢物的变化与相应的中药化学成分进行关联,同时如何将不同平台的中药代谢组学结果进行整合,以及如何将中药代谢组学结果与基因组学、转录组学、蛋白组学等其他的系统生物结果进行有机的整合,通过形成一套完整的整体组学策略,来研究中药复方的多靶点、多效应,如何建立完全符合中医特点的、整体观念的研究理论,如何选择药效学指标以全面反映多功效中药的各种临床疗效等,是中药药代动力学-代谢组学亟待解决的问题[26,33]。
3、药代动力学与药效动力学结合研究方法
PK-PD模型前者为阐明药物在体内的吸收、分布、转化和排泄过程及经时动力学过程,后者描述药物效应随时间变化的特征,采用数学模型将两个动力学过程整合,即将药物在体内的经时变化(时间-浓度)及其对生物机体对效应结合起来,可以更加准确地评价药物在体内的动力学过程和产生药理效应的动态变化,有助于全面系统地解答中药物质基础及其作用机制,该法已逐渐成为中药药代动力学研究的热点方法。目前PK-PD模型主要有以下几种:线性模型、对数线性模型、最大效应模型和SigmoidEmax模型、Sheiner效应模型、Paalzow效应模型、多重受体反应理论[34]。其中,药效学模型大多采用SigmoidEmax模型模型。为了表征中药整体PK/PD行为,郝海平[35]首次提出“中药多组分整合药代动力学研究”。该研究思路在血塞通注射液及脉络宁注射液的临床试验得以应用,提出了血塞通注射液的优化临床给药方案,初步证明中药的药代动力学研究在临床中药制剂给药方案设计与优化中应用的可行性和重要意义。但科学评价中药的整体PK/PD特征仍需进一步探索新的模型整合研究方法。
通过对中药活性成分的PK-PD相关性进行统计分析,可获得药物暴露量与药理效能之间的关系,可以指导中药新药的研发及临床安全性和有效性的评估。对于药效物质基础尚不明确的中药,采用药动学和药效学结合的方法,需要在众多有效成分中,选择与复方整体药效相关性较高的成分,来表征复方总体药代动力学的特征在实际研究中难度较大。同时,中药作用通路广泛,选择合适关乎药效的指标至关重要。
4、生物效应法
生物效应法是研究中药复方药代动力学的常用的方法,尤其针对成分不明确的中药复方。生物效应法体现了中药复方的整体观思想,符合中医基础理论。主要有药理效应法、药物累积法、微生物指标法,如表1所示。
表1生物效应法研究内容及特点[35,36]

05
中药药物相互作用研究
中药通过多成分多靶点模式发挥良好中医药整体治疗作用,中药多组分间会产生广泛的代谢/转化,并且中药多成分间的相互作用同样会使中药有效单体成分的药动学和药效学产生改变。中药可以通过多种机制引起对药物代谢酶和转运体产生作用,当生物体药酶/转运体系统发生改变时,会使得药物的体内处置与动力学特征发生改变,进而影响药效作用甚至产生毒副反应[6,33],药代动力学的药物相互作用主要是通过对药物代谢酶或转运体的抑制和诱导作用、或通过与肠道微生物发生相互作用而产生,这种相互作用可能发生于中药单体成分在体内吸收、分布、代谢、排泄任意一个环节,进而影响药物的体内过程,见表2。此外,中药会通过影响胃肠道pH环境改变联用药物的离子状态,从而改变其吸收程度;还可能通过影响pH敏感转运体(如OATP)的改变影响联用药物吸收;中药还能通过调节胃排空以及与血浆蛋白竞争性结合影响联用药物的PK特征;此外,中药可能还通过损伤肝或/和肾功能影响联用药物的消除。
表2中药衍生组蛋白去乙酰酶抑制剂(HDIs)的药代动力学机制[6]

通常中药产生的相互作用危害较低,并且停药后便可消失。但是,众多研究结果存在互相矛盾的现象。有学者[6]建议,首先需要建立标准化的生产规范,统一名称,不仅仅是中药的名称,还有拉丁名。第二,需要规范标准化提取方法,需要严格控制质量,鉴于临床常用煎煮剂,所以采用水提物更具临床意义。第三,实验所选的评价系统较为重要,例如,推荐基于人组织和细胞的系统。另外,对于中药粗提物,肝细胞或者肝微粒体系统不适用,第四,进行研究时应关注组织中药物的暴露水平,而不是血浆药物暴露水平。最后,应全面解读获得的结果,不能仅通过80-125%这个区间评判药物在人体上潜在的相互作用。
06
中药的生物分析方法
中药复方化学成分的复杂性和多样性、中药配伍的变异性和机体状态的不可预测性,给中药药代动力学研究带来了诸多问题[35],而中药进入体内发挥疗效的活性形式如果能被定性、定量可能是了解其体内过程的前提。因此,建立在复杂体系中实现分离、分析待测物的生物样本分析技术,是开展中药药代动力学研究的关键所在。随着现代分析技术和仪器的发展,如高效液相色谱-质谱联用技术、气相色谱-质谱联用、飞行时间质谱、离子淌度质谱以及生物样品前处理、在线分离等技术,使得复杂多样的、痕量药效活性成分在体内的定性、定量分析得以实现。除此之外,还有酶联免疫法、毛细管电色谱法、放射性标记法等用于中药药代动力学研究,极大地丰富了该研究领域的技术种类。绝大部分中药多成分药动学研究是对已有对照品的成分进行分析,随着色谱、质谱技术的发展,也随之涌现出来了半定量分析策略,可以应用于没有对照品时的体内药物分析。
液质联用技术是将色谱分离技术与质谱检测技术两者相结合,兼具色谱的分离能力和质谱的高灵敏度、高特异性以及抗干扰能力强等特点,可以应对中药复杂组分的快速检测、鉴定和准确定量,使其在中药药代动力学研究领域得到了广泛的应用。质谱按照质量分析器可分为:四极杆(Quadruple,简称Q)、离子阱(Iontrap,简称IT)、飞行时间质谱(Timeofflight,简称TOF)、轨道阱(Orbitrap)、线性离子阱-傅立叶变换-离子回旋共振(Lineariontrap-Fouriertransformioncyclotronresonance,简称LTQ-FTICR),以及将不同类型的质量分析器串联起来的复合式串联质谱,如的三重四极杆质谱(QQQ)、四极杆-飞行时间质谱(Q-TOF)(如图1所示)、离子阱-飞行时间质谱(IT-TOF)、液相色谱-核磁共振-质谱联用技术(Liquidchromatography-nuclearmagneticresonance-massspectrometry,简称LC-NMR-MS)。各类型质谱在中药的定性、定量研究中的比较如表3所示。

表3液相色谱/质谱法在中草药定性、定量分析中的比较[37]
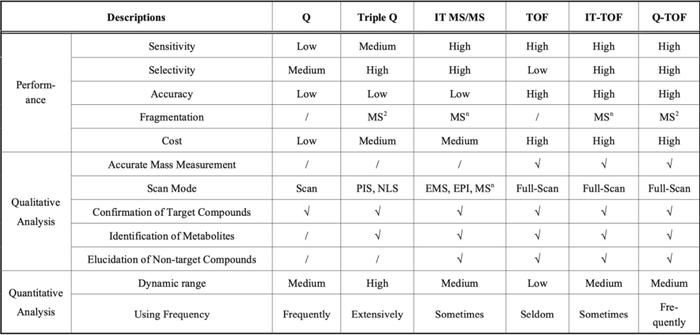
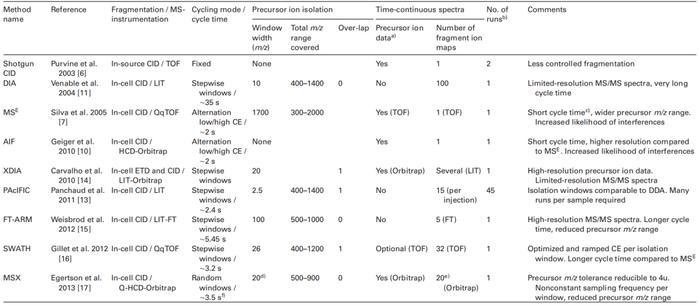
Orbitrap、Q-TOF、IT-TOF、LTQ-FTICR可以同时提供多级质谱信息以及高分辨质量数的数据,在中药及其代谢产物的结构鉴定的应用上具有绝对的优势,尤其,近年来数据的扫描模式从传统的数据依赖扫描模式(Datadependentacquisition,DDA)发展到数据非依赖扫描(Dataindependentacquisition,DIA)(如表4和图2所示)。通过MSE、MSALL技术(全分子量范围)、SWATH技术(Sequentialwindowedacquisitionofalltheoreticalfragmention)获得扫描范围内的全部粒子的碎片信息,具有强大的分辨率、扫描速率及高灵敏度等优势。
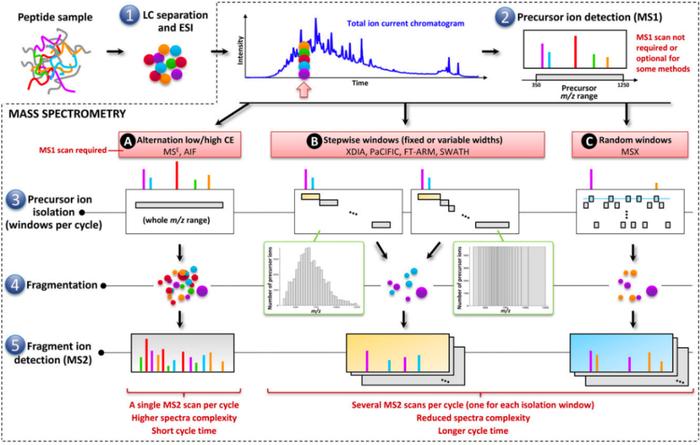
表4数据非依赖扫描计划[38]
1、定性策略
中药中的活性成分及其代谢产物的定性研究极具挑战,不光中药本身成分复杂,同时又引入生物基质的干扰,以及复杂的中药体系与人体相互作用后会产生丰富的代谢产物,使得该工作面临重重挑战。目前可结合通过标准品对照,质谱、核磁技术解析数据库筛选的方式。在已有标准品的情况下,可以通过化合物在色谱柱上的保留行为,如峰位、紫外吸收特征鉴定。但前提是需保证各成分间应达到基线分离。
先进的质谱技术可以提供丰富的质谱信息,可结合背景扣除技术对背景噪音进行扣减,以减少基质中的成分对待测物的干扰。运用背景扣除技术,可以识别淹没在背景信号中的微量或痕量物质。对于识别出来的未知成分根据碎片信息、准确的质量数信息以及碎片信息,结合质谱裂解的规律,结合先进的数据处理手段,如:质量亏损过滤、子离子过滤、中性丢失过滤以及同位素分布过滤等方法,确定分子式,推断化合物的结构。质谱解析工作量巨大,研究者们将中药的原型药物及其体内的代谢产物根据母核结构进行分类,具有相同母核结构的化合物可被归为一种类型,同一类型的化合物会具有相似的碎片离子和质谱裂解规律。通过软件总结不同类别化合物的特征碎片离子和质谱裂解规律,建立数据库,如基于诊断碎片离子扩展策略(Diagnosticfragment-ion-basedextensionstrategy)[39]。近年来,随着质谱技术的发展,结合组学研究手段,中药的定性分析上有了长足的进步。宋月林采用多维/多柱色谱-质谱联用结合多种扫描模式、在线能量分辨质谱(onlineER-MS)[40]、直接注射(DI)分析-拟靶向代谢组学等方法[41],建立了国际领先的中药化学成分高效分离与精确识别技术体系及其平台。
中药数据库可极大提高中药及其代谢产物鉴定的研究进程。目前,中药化学成分的数据库有TCMDatabase@Taiwan、TCMID、CEMTDD、SuperToxic和SuperNatural等。这些数据库能够提供包括中药中的成分、中药单方、中药复方的结构、代谢、靶点毒性等信息的检索服务。丰富和完善中药数据库的信息也是推动中药现代化进程的重要部分。
2、定量策略
化药的药代动力学的研究对象是通过选择药效和安全性相关的原型药或/和代谢产物确定的。前文已述,这对中药来说难度较大。通常,中药会通过测定药代指标成分来代表中药的整体药代动力学。药代指标成分可能是一个或几个药效明确、结构已知的活性组分、或者体内的代谢产物,并且它们与药效或/和安全性相关。王彩虹[42]总结了指标成分选择的方法:基于药代动力学特征选择指标成分、基于体内代谢途径选择药代指标成分、基于(预测的)药理活性(毒性)选择药代指标成分。确定了指标成分,即可采用液质联用技术进行检测,通过建立分析方法、对方法进行验证,然后应用于实际样品分析中。对于已知信息或假定信息可通过质谱不同的扫描模式有针对性地获取数据。质谱的扫描模式包括单离子监测扫描(Singleionmonitoring,SIM)、选择反应监测扫描(Selectivereactionmonitoring,SRM)、多反应监测扫描(Multi-reactionmonitoring,MRM)、母离子扫描、中性丢失扫描等。其中,MRM是对复杂混合物中目标物进行定量的重要技术手段,是质谱定量的金标准。近年来发展的ScheduledMRM(sMRM)模式可解决峰太细,扫描点数不够的问题,可实现大量化合物的准确MRM检测[43,44]。曹璐靖等[7]总结了基于HPLC-MS/MS、UPLC(UHPLC)-MS/MS和UFLC-MS/MS分析技术的中药提取物多成分(5种及以上)药代动力学研究概况,涵盖中药提取物中的黄酮类、生物碱类、萜类、皂苷类、酚酸类等一类或多类中药活性成分的药代动力学研究。
案
例
分
享
作为拥有集小分子、生物大分子于一体的PK/PD研究服务平台,阳光德美在中药的PK/PD研究中具有丰富的经验,如中药多组分药代动力学研究、流感病毒的qPCR检测以及抗抑郁中药的生物标志物研究等,部分案例分享如下。
案例一
中药千金藤素(Cepharanthine)具有广泛的药理活性,临床上应用于放化疗引起的白细胞减少症。2022年5月10日,中国科学家获得国家发明专利授权,专利说明书显示,体外实验10μM(微摩尔/升)千金藤素抑制冠状病毒复制的倍数为15393倍。阳光德美团队成员早在2009年开展了该药注射液的临床I期临床研究,建立了一种高效液相色谱-串联质谱(HPLC-MS/MS)快速、灵敏、特异测定人血浆中千金藤素的方法,通过AGILENTXDB-C8色谱柱进行分离,采用电喷雾电离(ESI)和多反应监测(MRM)在正离子模式下进行质谱分析,并通过优化前处理条件、流动相降低非同位素内标的干扰,定量下限达到了0.500ng/mL,成功应用于人体药代动力学研究。
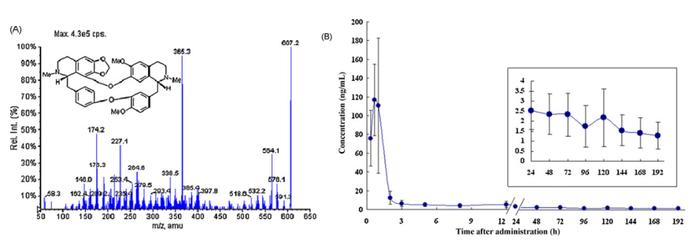
案例二
某中药制剂化学成分复杂,血浆中的干扰成分较多;需要同时检测两对同分异构体,共四个化合物,且给药后血浆中的浓度较低,需要很低的灵敏度,这些都对分析方法有极大的挑战。我们通过较缓的梯度和较严格的流动相能更有效的分离两对同分异构体和干扰组分。另外采用固相萃取的方法,一方面可以去除部分干扰,另一方面固相萃取与传统的液液萃取法相比较可以提高分析物的回收率,更有效地将分析物与干扰组分分离,减少样品预处理过程,使操作简单、省时、省力。
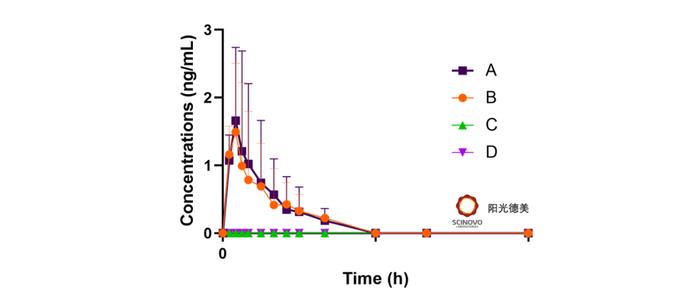
案例三
某中药制剂具有活血化瘀作用,临床用于预防和治疗心脑血管疾病。我们通过对流动相和色谱柱前处理的优化,实现了使用非同位素内标也能满足检测需求,且线性范围达900倍。还通过优化前处理条件、流动相、色谱柱等,解决了基质效应,极大地提高了灵敏度。同时采用了沉淀蛋白的前处理方法,比文献的固相萃取方法更节约成本。
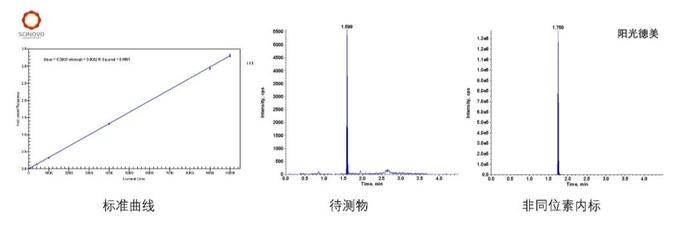
案例四
某中药颗粒临床用于治疗流行性感冒,通过采集口咽拭子检测流感病毒抗原阳性筛选受试者,并以流感病毒核酸转阴率作为疗效指标之一。我们采用实时荧光定量PCR法对口咽拭子中提取得到的核酸进行扩增,通过与CutPoint值对比,进行病毒核酸阴阳性的判断(如图6所示)。
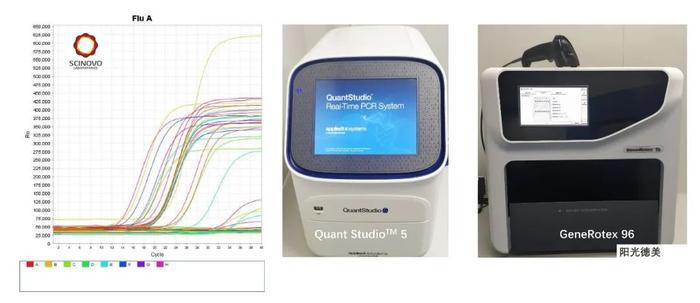
案例五
某中药提取物具有一定的镇静、抗抑郁作用,在研究其给药后对神经因子生物标志物浓度水平的影响实验中,我们采用数字式单分子免疫阵列分析仪(Simoa)建立了检测血清中Tau、pTau181、Aβ40和Aβ42浓度的方法。该方法的难点之一是筛选既能达到检测目的、又适用于数字式单分子免疫阵列分析仪的抗体对;二是解决基质效应与方法灵敏度的相对关系问题。我们在保证足够的灵敏度的前提下,通过预处理或稀释等方法消除了基质效应。
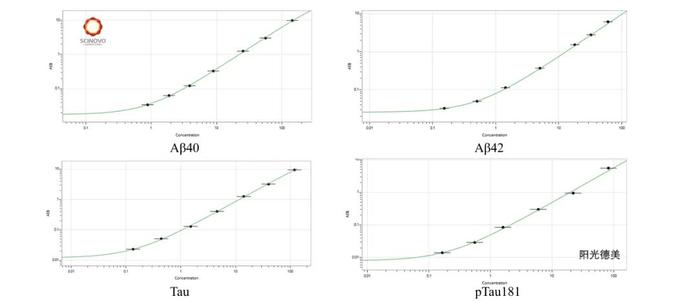
07
结语
传统中药是中华民族长期临床实践总结,因其来源于大量临床实践与应用,安全性和有效性具有保证。经科学家们的不懈探索,中药药代动力学研究已经取得了一定的进展,但仍不足以揭示中医药内涵,整体观是中药用药的精髓所在,也是中药药代动力学研究应当遵循的指导思想。相信随着现代科学技术的发展,中药研究在中医药理论的指导下,在尊重传统经验与临床实践相结合的前提下,建立符合中医理论的中药药代动力学的研究体系,最终阐明多组分、多靶点、多效应的科学内涵。中药必将会走出具有中国特色发展之路,走出国门、走向世界。
参考文献:
国家药典委员会.中华人民共和国药典:2020年版[M].化学工业出版社,2020.
刘昌孝.中药药代动力学研究的难点和热点[J].药学学报,2005,40(5):7.
巩仔鹏,林朝展,韩立炜.从国家自然科学基金资助项目浅析中药药代动力学研究现状[J].中国中药杂志,2021,46(4):7.
阳长明.中药复方新药研究的质量设计、质量完善与技术审评的分阶段要求[J].中草药,2017,48(16):6.
李川,中药药代动力学及其研究方法,第三届中医科学大会文集,7.
MaBL,MaYM.Pharmacokineticherb–druginteractionswithtraditionalChinesemedicine:progress,causesofconflictingresultsandsuggestionsforfutureresearch[J].DrugMetabolismReviews,2016:22.
曹璐靖,詹淑玉,姬翔宇,等.近五年中药提取物多成分药代动力学研究进展[J].中国中药杂志,2021,46(13):9.
ShanJJ,ZouJS,XieT,etal.EffectsofGancaoonpharmacokineticprofilesofplatycodinDanddeapio-platycodinDinJiegeng[J].JournalofEthnopharmacology,2015,170,50.
XiaoB,SunZ,SunSY,etal.Effectofcortexmorionpharmacokineticprofilesofmainisoflavonoidsfrompuerarialobatainratplasma[J].JournalofEthnopharmacology,2017,209,140.
XiaZ,LvL,DiX,etal.Thecompatibilityofsixalkaloidsinermiaopillexploredbyacomparativepharmacokineticandnetworkpharmacologicalstudy[J].BiomedicalChromatography,2019,33(5):e4509.
ZhangQ,LiY,LiuM.,etal.CompatibilitywithPanaxnotoginsengandRehmanniaglutinosaAlleviatestheHepatotoxicityandNephrotoxicityofTripterygiumwilfordiiviaModulatingthePharmacokineticsofTriptolide[J].InternationalJournalofMolecularSciences,2018,19(1):305.
MaoY,PengL,AnK,etal.InfluenceofJiegengonPharmacokineticPropertiesofFlavonoidsandSaponinsinGancao[J].Molecules,2017,22(10):1587.
ZhouB.,ZhangJ.,etal.TheinfluenceofcompatibilityofprocessedradixAconitiKusnezoffiionthepharmacokineticoffourcomponentsinGlycyrrhizauralensisFisch[J].JournalofEthnopharmacology,2015,169:1.
狄亚维.三七蒸制前后主要活性成分体内药动学及其抗血小板聚集活性比较研究[J].中草药,2016,47(1):6.
LeiT,ZhangD,GuoK,etal.ValidatedUPLC-MS/MSmethodforsimultaneousquantificationofeightsaikosaponinsinratplasma:Applicationtoacomparativepharmacokineticstudyindepressionratsafteroraladministrationofextractsofrawandvinegar-bakedBupleuriRadix[J].JournalofChromatographyB,2017,1060:231-239.
ZhangJ,FuY,LiL,etal.PharmacokineticcomparisonsofmajorbioactivecomponentsafteroraladministrationofrawandsteamedrhubarbbyUPLC-MS/MS[J].JPhamBiomedAnal,2019,171:43.
WeiG,LiJC,JiD,etal.PharmacokineticComparisonsofTypicalConstituentsinCurcumaeRhizomaandVinegar-ProcessedCurcumaeRhizomaafterOralAdministrationtoRats[J].Evidence-BasedComplementrayandAlternativeMedicine,2018:1.
TaoY,SuD,LiW,etal.Pharmacokineticcomparisonsofsixcomponentsfromrawandvinegar-processedDaphnegenkwaaqueousextractsfollowingoraladministrationinratsbyemployingUHPLC-MS/MSapproaches[J].JournalofChromatographyB,2018,1079:34.
LypB,YswA,XhlB,etal.PharmacokineticcomparisonoffivexanthonesinratplasmaafteroraladministrationofcrudeandprocessedGarciniahanburyiextracts[J].JournalofChromatographyB,2019,1126-1127:121737.
JiangH,YangL,XingX,etal.AsimpleliquidchromatographycoupledwithtandemmassspectrometryapproachforthesimultaneousquantificationofthirteencompoundsinratsfollowingoraladministrationofrawandprocessedFructusXanthii:Applicationinacomparativepharmacokineticstudy[J].JournalofSeparationScience,2019,42(22):3403.
王琰,蒋建东.肠道菌与药物代谢[M],科学出版社,2022
YangX.KeyfoundationalscienceprobleminexperimentalmedicinestudyofChinesemateriamedica:AscertainmentofactiveandtoxicconstituentsfromChinesemateriamedica[J].JournalofChineseIntegrativeMedicine,2005,3(2):154.
王海南.中药新药临床试验的特点和难点[J].中国中西医结合杂志,2007,27(7):3.
梁末雯.灯盏细辛注射液对脑缺血再灌注模型大鼠的PK-PD相关性研究[D].成都:成都中医药大学,2016:69.
束云,李连达.药代动力学-药效动力学结合模型在中药研究中的应用[J].中国药理学通报,2008,24(11):14.
李明会,阮玲玉,赵文龙,等.基于代谢组学/药动学整合策略的多组分中药药效物质基础研究[J].世界科学技术:中医药现代化,2018,20(8):5.
屠鹏飞,史社坡,姜勇.中药物质基础研究思路与方法.中草药,2012,43(2):209.
LuL,ShiW,Qing-XiaX,etal.Poly-pharmacokineticstrategyrepresentedthesynergyeffectsofbioactivecompoundsinatraditionalChinesemedicineformula,SiShenWananditsseparatedrecipestonormalandcolitisrats[J].Journalofseparationscience,2021,44(10):2065.
毕京峰,阎博华,魏振满.对当前复方中药药代动力学研究方法学的再评价[C]//全国临床药理学学术大会.2012:338.
罗国安,梁琼麟,刘清飞,等.整合化学物质组学的整体系统生物学——中药复方配伍和作用机理研究的整体方法论.世界科学技术:中医药现代化,2007,9(1):10.
郭立玮,朱华旭,潘林梅.基于复杂体系原理的中药复方药效物质“组合筛选”思路与方法[J].中草药,2009,40(4):505.
孙宇飞.基于PK-PD关联分析研究定志小丸治疗阿尔茨海默病的药效物质基础及作用机制[D].中国科学技术大学.
杨中良,胡庆禧,周怡,等.代谢组学在中医中药领域的应用进展、问题及对策[J].中国中医药科技,2014(6):3.
李雪溦,张红阳,朱继孝.中药复方药物代谢动力学研究进展[J].中医药通报,2015,14(5):5.
郝海平,郑超湳,王广基.多组分、多靶点中药整体药代动力学研究的思考与探索[J].药学学报,2009,44(3):270.
裴利霞.中药药物动力学研究集粹[J].中医药学刊,2005,23(1):3.
WuL,HaoH,WangG.LC/MSBasedToolsandStrategiesonQualitativeandQuantitativeAnalysisofHerbalComponentsinComplexMatrixes[J].CurrentDrugMetabolism,2012,13(9):1251.
BilbaoA,VaresioE,LubanJ,etal.Processingstrategiesandsoftwaresolutionsfordata-independentacquisitioninmassspectrometry[J].Proteomics,2015,15(5-6):964.
ZhengC,HaoH,WangX,etal.Diagnosticfragment‐ion‐basedextensionstrategyforrapidscreeningandidentificationofserialcomponentsofhomologousfamiliescontainedintraditionalChinesemedicineprescriptionusinghigh‐resolutionLC‐ESI‐IT‐TOF/MS:Shengmaiinjectionasanexample[J].JournalofMassSpectrometry,2009,44(2):230.
GuanPW,LiuWJ,CaoY,TangHT,etal.FullCollisionEnergyRamp-MS2SpectruminStructuralAnalysisRelyingonMS/MS.Anal.Chem.2021,93(46):15381.
ZhangK,LiuW,SongQ,etal.IntegratedStrategyDrivesDirectInfusion-TandemMassSpectrometryasanEligibleToolforShotgunPseudo-TargetedMetabolomicsofMedicinalPlants.AnalChem.2021.93,4,2541.
王彩虹.中药多成分药代动力学的新方法和策略研究[D].北京协和医学院,2017.
SongQ,SongY,ZhangN,etal.Potentialofhyphenatedultra-highperformanceliquidchromatography-scheduledmultiplereactionmonitoringalgorithmforlarge-scalequantitativeanalysisoftraditionalChinesemedicines[J].RSCAdvances,2015,5.
SongY,SongQ,LiJ,etal.Anintegratedstrategytoquantitativelydifferentiatechemome betweenCistanchedeserticolaandC.tubulosausinghighperformanceliquidchromatography-hybridtriplequadrupole-lineariontrapmassspectrometry[J].JournalofChromatographyA,2016:238.
HaoG,LiangH,LiY,etal.Simple,sensitiveandrapidHPLC–MS/MSmethodforthedeterminationofcepharanthineinhumanplasma[J].JournalofChromatographyB,2010,878(28):2923-2927.
46.数据来源于阳光德美.
北京阳光德美医药科技有限公司
北京阳光德美医药科技有限公司成立于2016年11月,属于阳光诺和(股票代码:688621)全资子公司,是一家集大/小分子药物分析为一体的、覆盖临床前到临床全链条的PK/PD研究平台和生物分析平台,可为国内外客户提供国际化水准的、以临床价值和患者需求为导向的创新药项目研发服务,包括:药代动力学生物分析服务、免疫原性生物分析服务、药效学和生物标志物研究服务及定量药理学研究服务。 专注于解决客户药代药效研究及生物分析中所遇到的挑战,致力于打造国内领先的集大、小分子创新药物临床前以及临床研究于一体的生物分析和PK/PD研究平台。
