正大天晴超5000万美元引进,口服PPAR激动剂在中国获批临床
转自:医药观澜
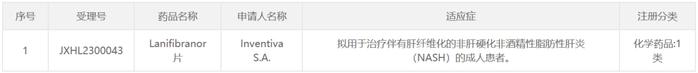
近日,中国国家药监局药品审评中心(CDE)官网公示,Inventiva公司申请的1类新药lanifibranor片获得临床试验默示许可,拟开发用于治疗伴有肝纤维化的非肝硬化非酒精性脂肪性肝炎(NASH)的成人患者。公开资料显示,lanifibranor(拉尼兰诺)是一种口服PPAR激动剂,正大天晴通过一项超5000万美元的合作,获得了该药在大中华区的开发、生产和商业化权利。
Lanifibranor是一种口服过氧化物酶体增殖物激活受体(PPAR)激动剂,可同时激活PPARα、PPARδ和PPARγ,这些受体在调控脂质代谢、炎症反应和纤维化过程中发挥重要作用。该药物通过作用于这三种PPAR亚型来调节脂肪代谢,减轻肝脏炎症和纤维化。此前,美国FDA已授予lanifibranor用于治疗NASH的突破性疗法认定和快速通道资格。
2022年9月,正大天晴与Inventiva公司签订许可协议,获得了lanifibranor在大中华区(包括中国大陆、香港、澳门、台湾地区)的独家许可。根据协议,正大天晴将向Inventiva公司支付1200万美元的首付款及最高不超过4000万美元的潜在的临床及注册里程碑付款。

此次lanifibranor在中国获批临床,拟开发用于非肝硬化NASH成人患者。NASH是非酒精性脂肪性肝病(NAFLD)的更晚期形式,也是导致肝脏相关死亡的主要原因。此外,NASH患者,特别是那些具有更多代谢风险因素的患者,心血管不良事件的风险增加,发病率和死亡率也相应提高。一旦NASH发展为显著的肝纤维化,患者产生不良肝损伤结果的风险急剧上升。
此前,在针对NASH的2b期NATIVE试验中,lanifibranor已显示出良好的安全性和耐受性。lanifibranor1200mg/天、持续24周的治疗,显著降低了肥胖且经活检证实为NASH患者的SAF-A(脂肪变性、活动性、纤维化的活动度)评分。此外,研究也达到了多个次要终点,包括NASH缓解且纤维化不进展,纤维化分期改善至少1期且NASH无恶化,以及NASH缓解且纤维化分期至少改善1期。此外,lanifibranor治疗还显著改善了血清转氨酶水平,肝损伤、炎症和纤维化的生物标志物,糖化血红蛋白(HbA1c)、脂质水平和胰岛素水平。该试验结果已于2021年10月在《新英格兰医学杂志》(NEJM)发表。
根据ClinicalTrials网站,目前lanifibranor正在开展多项中后期临床试验。其中,包括治疗NASH和肝纤维化2期或3期成人患者的3期临床试验,以及治疗NASH或NAFLD合并2型糖尿病患者的2期临床试验。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.RetrievedMay 22 ,2023.From https://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731
[2]中国生物制药引进潜在BICNASH口服药物lanifibranor.RetrievedSep22,2022.Fromhttps://mp.weixin.qq.com/s/kRBYh5WFe_P6u3h8S4jzjA
[3]GuadalupeGarciaTsao.NonalcoholicSteatohepatitis—OpportunitiesandChallenges.RetrievedOctober21,2021,fromhttp://www.nejm.org/doi/full/10.1056/NEJMe2110989
