速递 | 晚期癌症OS和PFS几乎翻倍!重磅ADC/Keytruda组合疗法3期结果登《新英格兰医学杂志》
转自:药明康德
近日,由安斯泰来(Astellas)和辉瑞(Pfizer)旗下Seagen公司所开发的抗体偶联药物(ADC)Padcev(enfortumabvedotin)联用默沙东(MSD)PD-1抑制剂Keytruda(pembrolizumab)一线治疗局部晚期或转移性尿路上皮癌(la/mUC)成人患者的3期临床试验结果在《新英格兰医学杂志》(NEJM)上发表。结果表明,Padcev联用Keytruda一线治疗la/mUC患者的生存结局明显优于化疗,安全性与既往报道的一致。

这是一项在886例既往未接受过全身性治疗的la/mUC患者中开展的开放标签、随机化3期临床试验EV-302/KN-A39,患者以1:1的比例随机接受吉西他滨联合顺铂或卡铂(n=444)或Padcev联合Keytruda(n=442)的治疗。主要疗效结局指标为设盲独立中心审评所分析的总生存期(OS)和无进展生存期(PFS)。
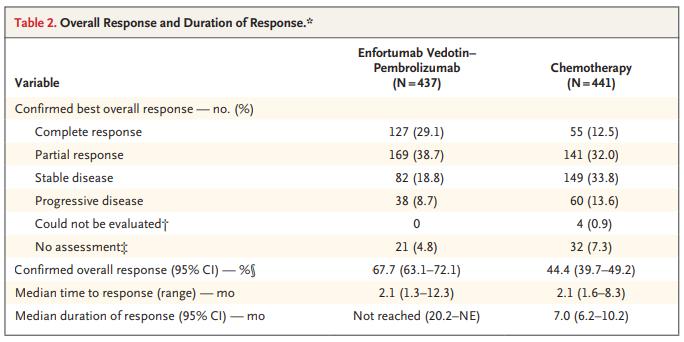
截至2023年8月8日的数据,接受Padcev联合疗法患者的确认的总缓解率(ORR)为67.7%(95%CI:63.1-72.1),高于含铂化疗组的44.4%(95%CI:39.7-49.2),p<0.001。在Padcev联合治疗组中,29.1%的患者获得了完全缓解,在含铂化疗组中,这一比例为12.5%。Padcev联合治疗组的缓解持续时间(DOR)的中位数尚未达到,化疗组的DOR为7.0个月。Padcev联合治疗组中,12个月和18个月时仍处于缓解状态的患者比例分别为67.3%和59.6%,而在化疗组中,这一比例分别为35.2%和19.3%。
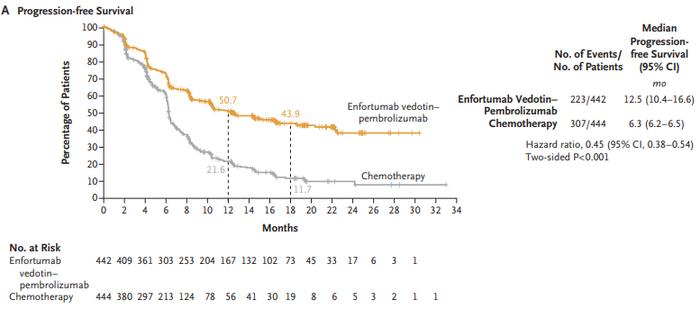
生存期的中位随访时间为17.2个月时,与含铂化疗方案相比,接受Padcev与Keytruda联合疗法患者的OS和PFS均出现统计学显著性改善。接受Padcev联合疗法患者的中位PFS为12.5个月(95%CI:10.4-16.6),接受含铂化疗患者的中位PFS为6.3个月(95%CI:6.2-6.5),即与化疗相比,联合疗法组患者的PFS显著延长,疾病进展或死亡风险降低了55%(HR:0.45,95%CI:0.38-0.54,p<0.001)。
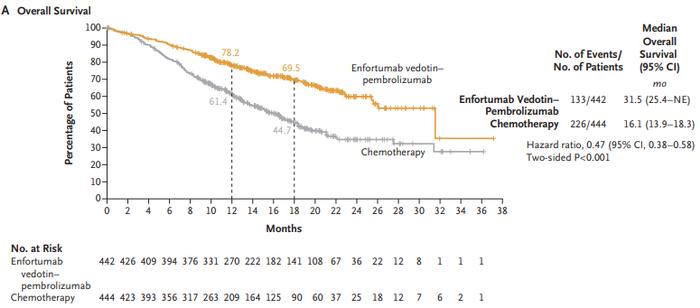
接受Padcev联合疗法患者的中位OS为31.5个月(95%CI:25.4-无法估计),接受含铂化疗治疗患者的中位OS为16.1个月(95%CI:13.9-18.3),即与化疗组相比,联合疗法组患者的死亡风险降低53%(HR:0.47,95%CI:0.38-0.58,p<0.001)。
安全性方面,55.9%的联合疗法组患者发生了≥3级治疗相关的不良事件(TRAE),此数值在化疗组中为69.5%。
Padcev是一种抗体偶联药物,其靶点为Nectin-4,这是一种位于细胞表面并在膀胱癌中高表达的蛋白质。临床前数据表明,这种药物的抗癌活性是由于它与表达Nectin-4的细胞结合,然后将抗肿瘤药物MMAE内化并释放到细胞中,导致细胞不再增殖(细胞周期停止)并出现程序性细胞死亡(凋亡)。
Keytruda是一种PD-1单克隆抗体,可阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,从而激活T淋巴细胞,以发挥抗肿瘤功效。2023年4月,美国FDA根据EV-103试验的结果,加速批准Padcev联合Keytruda治疗不适合接受含顺铂化疗的la/mUC成人患者。
