恒瑞创新药卡瑞利珠单抗联合方案用于初始不可切非小细胞肺癌研究荣登《STTT》
转自:恒瑞医药
近日,同济大学附属上海市肺科医院姜格宁、张鹏教授团队开展的一项探索卡瑞利珠单抗联合化疗或阿帕替尼的新辅助治疗对初始不可切除NSCLC疗效的研究全文发表于《自然》子刊、国际知名医学期刊《SignalTransductionandTargetedTherapy》(STTT,IF=39.3)1。该研究探索了卡瑞利珠单抗联合治疗方案是否可以使更多初始不可切除非小细胞肺癌(NSCLC)患者有手术获益的机会。结果表明1,卡瑞利珠单抗联合化疗组手术率为50.0%,卡瑞利珠单抗联合阿帕替尼治疗组手术率为42.9%,所有手术患者均实现了R0切除,有望为局部晚期NSCLC患者带来新的治疗策略。

研究文章发表于《SignalTransductionandTargetedTherapy》
研究背景
肺癌是全球发病和死亡人数最多的恶性肿瘤之一,其中非小细胞肺癌(Non-smallcelllungcancer,NSCLC)占比约85%2。约半数NSCLC患者确诊时处于疾病早期或局部晚期2,根据是否可手术完整切除,又进一步分为可切除、潜在可切除和初始不可切除疾病。对于初始不可切除NSCLC患者,目前标准治疗方案为同步放化疗加免疫巩固治疗。随着研究的深入,越来越多的证据表明3-5,新辅助免疫联合治疗能显著提高可切除NSCLC患者的病理完全缓解(pCR)率和无事件生存期(EFS)。然而,新辅助免疫联合治疗能否将初始不可切除NSCLC转化为可切除状态,从而使该部分患者具备手术机会,仍缺乏前瞻性研究证据。
基于医学界对于初始不可切除NSCLC缺乏明确的定义这一临床问题,姜格宁、张鹏教授团队结合国内外专家共识及上海市肺科医院胸外科的经验,成立了多学科临床专家组(Multidisciplinaryclinicalteam,MDT)共同制定了初始不可切除NSCLC的“肺科定义”:(1)肿瘤侵犯大血管、气管或主支气管等重要结构,术前评估判断诱导治疗降级后有以治愈为目的的切除机会的患者;(2)临床证实的淋巴结呈多站转移或巨块型融合,术前评估判断诱导治疗降级后能够耐受并进行肺门和纵隔淋巴结清扫术的患者;(3)术前评估认为即使行全肺切除,特别是右全肺切除,也有不能R0切除的可能。满足以上三个条件中任何一个即为初始不可切除NSCLC。
研究方法
从2020年9月29日至2022年6月29日,该研究共纳入51例初始不可切除的、EGFR及ALK阴性的Ⅱ-Ⅲ期初治NSCLC患者,其中30例接受卡瑞利珠单抗联合化疗(A组),21例接受卡瑞利珠单抗联合阿帕替尼治疗(B组)。经过2-4个周期新辅助治疗后,由多学科诊疗(MDT)评估为可切除的患者接受手术治疗,否则接受根治性放疗。主要研究终点为主要病理缓解(MPR)率。
研究结果
结果表明,A组手术率为50.0%(15/30),B组手术率为42.9%(9/21),所有手术患者均实现了R0切除。在手术患者中,A组的MPR率和pCR率均为20.0%,B组分别为55.6%和11.1%。两组患者的客观缓解率(ORR)分别为33.3%和55.6%。在22.4个月的中位随访期内,A组的中位EFS未达到,B组的中位EFS为16.8个月。安全性方面,与既往报道的新辅助免疫联合治疗相近。整个研究过程中未出现治疗相关死亡事件,无新辅助治疗相关手术推迟,无术后90天内死亡病例,整体安全性可控且可耐受。
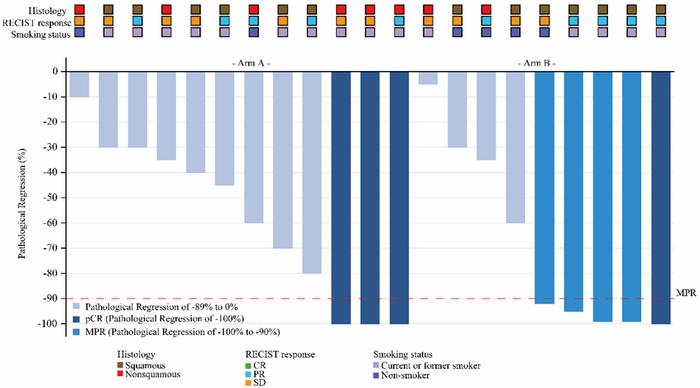
新辅助免疫联合治疗后的病理缓解情况
此外,该研究还探索了对新辅助卡瑞利珠单抗联合阿帕替尼治疗敏感的生物标志物。通过对13例患者基线肿瘤样本的分析,研究者发现TYROBP在应答者中显著高表达,且其较PD-1和PD-L1具有更好的治疗应答预测效能(AUC=0.909),高表达TYROBP的患者具有更好的EFS和OS。这一发现在多个已发表的公开数据集中亦得到验证6-9。进一步的基因富集分析(Genesetenrichmentanalysis,GSEA)表明,“interferongammaresponse”、“NKcell-mediatedcytotoxicity”和“antigenprocessingandpresentation”等通路在治疗应答者中显著富集。此外,应答者的肿瘤中有更高水平的免疫评分和CD8+T细胞浸润,且T细胞相关基因CCL5、NKG7亦显著高表达。提示TYROBP可能与治疗响应相关。
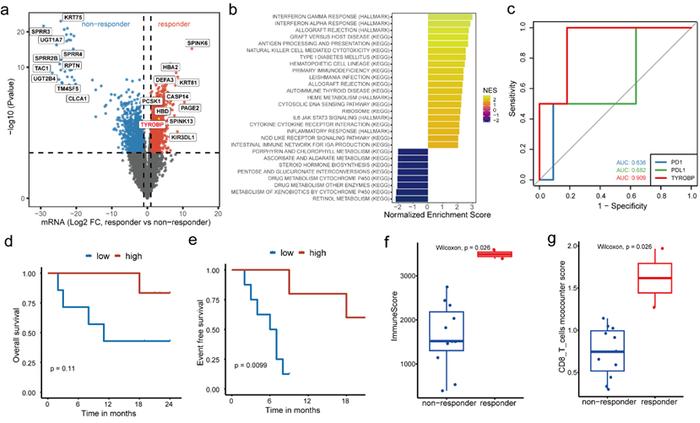
基线肿瘤样本RNA-seq探索对于治疗应答的生物标志物
研究总结
该研究首次明确定义了初始不可切除NSCLC,并初步证明了新辅助卡瑞利珠单抗联合化疗或阿帕替尼对该类人群疗效良好且安全性可控,将不可切NSCLC患者转化为可进行手术状态,从而有望为局部晚期NSCLC患者带来新的治疗策略。对生物标志物的探索表明,TYROBP可能是免疫联合阿帕替尼治疗应答的有效预测指标,有望指导临床筛选潜在获益人群。
参考文献:
1.Xia,H.,Zhang,H.,Ruan,Z.etal.Neoadjuvantcamrelizumab(ananti-PD-1antibody)pluschemotherapyorapatinib(aVEGFR-2inhibitor)forinitiallyunresectablestageII–IIInon-small-celllungcancer:amulticentre,two-arm,phase2exploratorystudy.SigTransductTargetTher9,145(2024).https://doi.org/10.1038/s41392-024-01861-w.
2.Bourreau,C.,Treps,L.,Faure,S.,Fradin,D.&Clere,N.Therapeuticstrategiesfornon-smallcelllungcancer:Experimentalmodelsandemergingbiomarkerstomonitordrugefficacies.Pharmacol.Ther.242,108347(2023).
3.Forde,P.M.etal.NeoadjuvantNivolumabplusChemotherapyinResectableLungCancer.N.Engl.J.Med.386,1973-1985(2022).
4.Wakelee,H.etal.PerioperativePembrolizumabforEarly-StageNon-Small-CellLungCancer.N.Engl.J.Med.389,491-503(2023).
5.Lu,S.etal.PerioperativeToripalimabPlusChemotherapyforPatientsWithResectableNon-SmallCellLungCancer:TheNeotorchRandomizedClinicalTrial.JAMA.331,201-211(2024).
6.Wu,P.,Xiang,T.,Wang,J.,Lv,R.&Wu,G.TYROBPisapotentialprognosticbiomarkerofclearcellrenalcellcarcinoma.FEBSOpenBio.10,2588-2604(2020).
7.Jiang,J.etal.IdentificationofTYROBPandC1QBasTwoNovelKeyGenesWithPrognosticValueinGastricCancerbyNetworkAnalysis.Front.Oncol.10,1765(2020).
8.Shabo,I.,Olsson,H.,Stal,O.&Svanvik,J.BreastcancerexpressionofDAP12isassociatedwithskeletalandlivermetastasesandpoorsurvival.Clin.BreastCancer.13,371-377(2013).
9.Dietrich,J.,Cella,M.,Seiffert,M.,Buhring,H.J.&Colonna,M.Cuttingedge:signal-regulatoryproteinbeta1isaDAP12-associatedactivatingreceptorexpressedinmyeloidcells.J.Immunol.164,9-12(2000).
