Cell | 揭示哺乳动物卵细胞储存早期胚胎发育所需的蛋白机制
转自:生物谷
哺乳动物生育后代时,它们会投入很多。与鱼或青蛙不同,胚胎无法自行发育。它必须植入子宫,并在那里获得生存所需的一切。在此之前,卵细胞一直在为早期胚胎提供营养。除其他外,它还提供必需的蛋白。
在一项新的研究中,德国马克斯-普朗克多学科科学研究所的MelinaSchuh领导的研究人员与哥廷根大学的同事一起,阐明了卵细胞是如何储存蛋白的。他们的实验还为了解蛋白储存错误如何导致不孕症提供了重要启示。令科学家们困惑了60多年的卵细胞结构在其中发挥了至关重要的作用。相关研究结果于2023年11月2日在线发表在Cell期刊上,论文标题为“Mammalianoocytesstoreproteinsfortheearlyembryooncytoplasmiclattices”。

对于许多夫妇来说,为人父母是一个漫长的过程。对有些人来说,生儿育女的愿望甚至仍未实现。病因多种多样,男性和女性都有。女性的生育能力会随着年龄的增长而下降,不孕不育的可能性也会增加。不过,基因突变也可能导致这种情况。
对全球不孕女性遗传物质的分析表明,导致女性不孕的最常见遗传原因之一是某些基因的突变。这些基因包含制造蛋白PADI6和称为皮质下母体复合体(SubcortialMaternalComplex,SCMC)的蛋白复合体的蓝图。然而,人们以前并不清楚这些蛋白在不孕症中的具体作用。
蛋白储存场所
Schuh及其研究团队如今利用成像技术可视化观察到,PADI6和SCMC是填充卵细胞内部结构的主要成分。Schuh解释说,“几十年来,研究界一直在困惑这种结构的功能和组成,我们称其为细胞质晶格(cytoplasmiclattices)。”
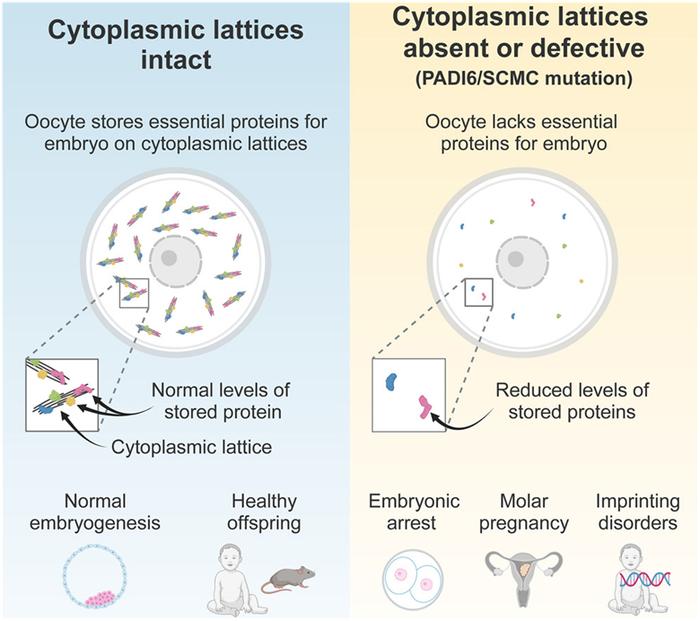
当这些作者从小鼠卵细胞中移除PADI6和SCMC蛋白时,细胞质晶格消失了---这带来了致命的后果。Schuh说,“缺乏细胞质晶格的小鼠卵细胞也缺乏早期胚胎所需的蛋白。胚胎的发育在受精后不久就停止了。因此,我们猜测细胞质晶格可能是蛋白的储存场所。”
在卵细胞中储存蛋白绝非易事。这是因为卵细胞是在雌性哺乳动物出生后的卵巢中产生的,并在卵巢中保持数月甚至数年的功能性。卵细胞必须在相应长的时间内储存蛋白,使之不被降解或在错误的时间变得活跃。
接下来,Schuh团队研究了细胞质晶格中含有哪些蛋白。他们与马克斯-普朗克多学科科学研究所的HenningUrlaub和JulianeLiepe领导的研究团队合作,利用质谱法和生物信息学确定了细胞质晶格中的确切蛋白含量。
他们的结果显示,细胞质晶格与许多对胚胎发育至关重要的蛋白结合。Schuh指出,“我们的结果有力地证明了我们的假设是正确的:细胞质晶格是卵细胞的蛋白储存场所,为早期胚胎提供重要的蛋白。”
PADI6和SCMC蛋白储存蛋白
他们进一步发现,PADI6和SCMC蛋白承担着为胚胎早期发育收集和储存蛋白的任务。论文第一作者IdaJentoft说,“这就解释了为什么如果这些蛋白缺失或无法发挥其功能,胚胎在受精后不久就会停止发育。我们当时感兴趣的是如果PADI6和SCMC因基因突变而缺失,是否可以替代有缺陷的蛋白储存场所。”
在实验中,这些作者成功地将这些缺失的细胞质晶格蛋白人为地重新引入到生长中的小鼠卵细胞中。通过这种方法,也有可能在有缺陷的人类卵细胞中重建细胞质晶格。Jentoft认为,这可能是治疗由PADI6和SCMC基因突变引起的不孕症的一种很有前景的新方法。
显微镜下冷冻的卵细胞
当被问及为什么花了几十年时间才破译出卵细胞中神秘的细胞质晶格结构的功能时,Schuh和Jentoft给出了一个简短的答案:卵细胞的大小和方法的缺乏。卵细胞是哺乳动物众多种细胞类型中的巨大细胞。卵细胞储存蛋白的特性决定了很难对其内部进行研究。
Schuh解释说,“方法学上的主要挑战是如何让卵细胞能够被我们使用的成像方法---高分辨率光学显微镜和低温电子断层扫描(cryo-ET)---观察到。cryo-ET可以在几乎自然的条件下对卵细胞的三维分子结构进行研究。这在以前是不可能实现的。”该团队在这一过程中取得的突破得益于生殖医学中一个屡试不爽的技巧。
对cryo-ET而言,细胞必须首先被急速冷冻。这些作者利用了诊所为人工授精定期冷冻人类卵细胞的做法来储存它们。为了在冷冻过程中保护卵细胞,诊所会使用冷冻保护剂。哥廷根大学医学中心的RubénFernández-Busnadiego报告说,“我们的想法是使用同样的冷冻保护剂来实现所需的卵细胞快速冷冻。”
Schuh补充说,“利用这种方法,我们可以研究卵细胞中的细胞质晶格,并开始详细解读它们的结构。”这些作者希望这些新技术能够在卵细胞研究领域取得重要进展,并在未来开发出新的治疗方法。
参考资料:
IdaM.A.Jentoftetal.Mammalianoocytesstoreproteinsfortheearlyembryooncytoplasmiclattices.Cell,2023,doi:10.1016/j.cell.2023.10.003.
Proteinstockforthebeginningofanewlifehttps://www.mpg.de/21055528/1106-bich-protein-stock-for-the-beginning-of-a-new-life-17216463-x
