免疫治疗真实世界报告出炉!疗效与生存质量并重
转自:医学界
精彩提要
1.免疫检查点抑制剂(ICIs)的使用与患者报告结局(PROs)评分改善有关。
2.包含ICIs的多药联合治疗未显示与其相关的健康相关生存质量(HRQoL)改善,但不会导致患者生存质量恶化。
3.免疫治疗有助于改善患者生存质量。
ICIs改变了肿瘤的治疗模式。尽管在过去几年中对ICIs的治疗效果进行了广泛的研究,但与其他抗癌治疗相比,其与患者生活质量的关系却少见报道。
2022年8月16日发表在JAMANetworkOpen上的一篇系统评价和荟萃分析中,基于多个纳入了接受或不接受免疫治疗的晚期实体瘤患者的随机临床试验(RCT),研究者详细分析了在其中评估的患者报告结局(PROs),以探索ICIs与实体瘤患者的生活质量之间的关系。

研究者在PubMed、MEDLINE、Embase和Scopus数据库中检索了与ICIs以及PROs相关的所有RCT研究,时间截止日期为2021年6月1日,共检索到2259项研究。研究者规定实验组为:使用ICIs为单一疗法或联合化疗或联合另一种ICIs和/或靶向治疗的实体瘤患者;规定对照组为:不包含免疫治疗的晚期实体瘤患者。
研究方法
研究检索纳入34项免疫治疗相关的研究文献,共包括18709名患者,研究涉及的ICIs包括PD-1抑制剂、PD-L1抑制剂和CTLA-4抑制剂。根据欧洲癌症研究与治疗组织(EORTC)核心生活质量问卷(QLQ-C30)的全球健康状况(GHS)量表,或EuroQol健康相关生活质量5维3水平(EQ-5D-3L)视觉模拟量表(VAS),评估PROs。研究者运用Cochrane偏差风险工具报告了试验的质量评估。
研究终点
(1)治疗组之间在通过QLQ-C30GHS或EQ-5D-3LVAS评估的PRO评分从基线到12和24周随访的平均变化方面的差异;
(2)治疗组之间在PRO评分恶化时间(TTD)方面的差异,定义为从患者随机化到临床相关性PRO评分首次恶化的时间,这是在整个试验随访期间评估患者生存质量(QoL)治疗效果的一种主要措施。
研究结果
在应用ICIs作为单药治疗的19个RCT中,PROs评分从基线到随访12周的平均变化的组间差异为4.6(95%CI,2.8~6.4),从基线到24周的平均变化为6.1(95%CI,4.2~8.1),PROs的变化结果显著支持ICIs可改善生活质量。
在应用ICIs联合化疗的8个RCT中,PROs评分在12周和24周的总差异分别为1.4(95%CI:−0.4~3.2)和2.5(95%CI:−0.8~5.9)。
在应用其他含ICIs治疗组合的8个RCT中,PROs评分在12周和24周的总差异分别为2.1(95%CI:−0.8~5.0)和2.1(95%CI,−0.4~4.5)。
所有3组评估的RCT中,与对照组相比,包含ICIs的治疗组的恶化时间明显更长[ICIs作为单药治疗的风险比为0.80(95%CI:0.70~0.91),ICIs联合化疗的风险比为0.89(95%CI:0.78~1.00),其他含ICIs的组合的风险比为0.78(95%CI:0.63~0.96)]。
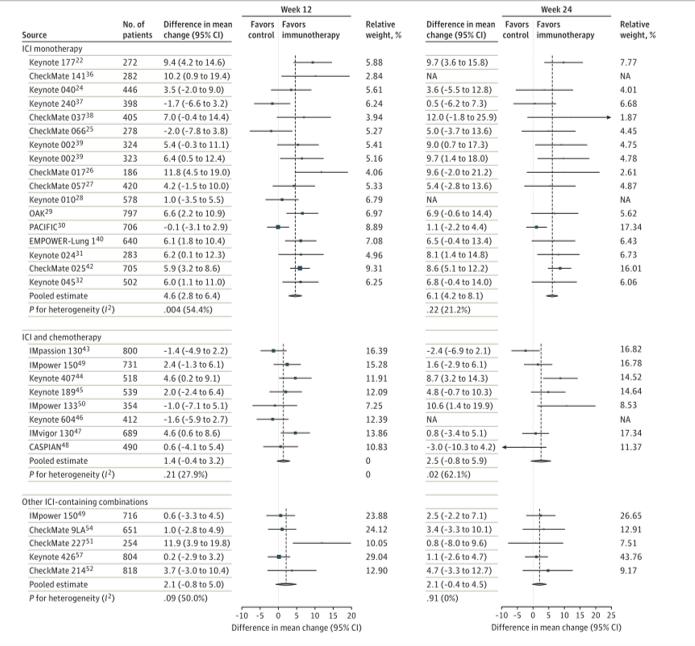
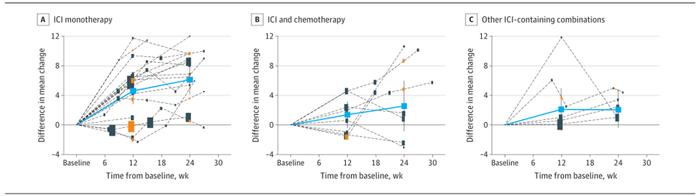
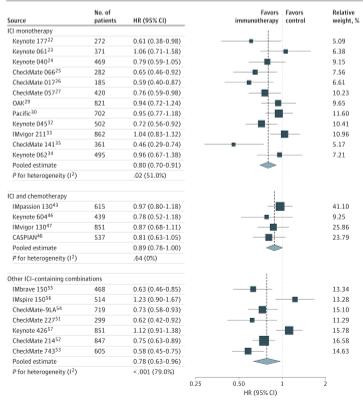
研究结果显示,在ICIs单药治疗RCT中,随着时间的推移,PROs的差异支持免疫治疗对于改善患者生存质量有益。然而,在ICIs与其他药物联合应用的RCT中,在12或24周时PRO改善程度是有限的,并且在临床相关的临界值以下。虽然这一结果不能得出在接受ICIs联合治疗的患者中存在更好的健康相关生存治疗(HRQoL)的结论,但它支持这样的结论:即与对照组相比,多药组合没有恶化患者的生活质量。考虑到在一些随机对照试验中,患者接受了多达3类不同类别的药物,这一发现值得注意。
研究结论
ICIs作为单药治疗似乎与患者报告的生活质量有良好的相关性,并且可以与其他类别的抗癌药物联合使用而不会降低生活质量的改善。
研究讨论
随着免疫治疗联合化疗正成为多种实体瘤的标准治疗,这项评估多种包含免疫治疗在内的实体瘤治疗方案对PROs的影响的荟萃分析显示出了深远的临床意义。
然而,研究者指出,在完成此系统综述的过程中出现的一个重要观察结果是,所纳入的RCT中没有一项将HRQoL作为主要终点,而通常只在次要终点和延迟报告中提及PROs。这一观察结果显示了对HRQoL在抗癌免疫治疗领域的重要性是被低估的。
对此,研究者提出了一些建议。首先,HRQoL的评估应包括在RCT检测免疫疗法的主要目标中。第二,应该更广泛地考虑联合评估疗效、毒性和HRQoL的联合终点,例如生存质量调整的无疾病或毒性症状时间(Q-TWiST),将PROs纳入试验结果的主要分析中,以实现对新治疗方法的风险-收益比的公正评估。此外,在大多数情况下,随机对照试验中的HRQoL评估在24周后停止,由于ICIs显著增加了长期存活患者的百分比,因此应该延长ICIs试验的计划随访时间,以完善HRQoL收集。最后,目前用于评估PRO的工具的具有局限性,由于缺乏专门的开发和验证,这些工具可能无法完全捕捉到某种新疗法的耐受性特征。因此,研究者建议专注于生存质量的相关科学协会应该加快针对免疫疗法试验的新HRQoL评估工具的开发、验证和推广。
另外,研究者指出了此研究的一些局限性。首先,此分析仅纳入已发表的研究,而不是个体病例数据(IPD)的Meta分析。其次,尽管研究者发现了可能与纳入RCT的患者的不同肿瘤组织类型有关的异质性。不同肿瘤组织类型的患者之间的潜在差异值得在未来进行更详细的研究。第三,由于到目前为止只有极少数RCT报道了在新佐剂或佐剂环境中测试ICIs的结果,研究者未将这些研究纳入此项分析。
研究拓展
目前,随着免疫治疗在肿瘤治疗领域的应用越来越为广大临床医生及研究者重视,免疫治疗药物长久以来一直是药物研发和临床试验的热点,相关的RCT层出不穷,与之伴随的是免疫治疗相关的Meta分析的不断涌现。
其中,除了免疫治疗在不同癌症种类中的疗效之外,受到研究者广泛关注,也是相关研究发表数量相当多的就是免疫治疗的安全性(包括药物毒性、免疫相关不良反应等)问题。
2018年一项Meta分析评估了与免疫检查点抑制剂相关的致命毒性作用,结果指出,免疫检查点抑制剂的致命毒性作用是罕见的,发生率约为0.3%~1.3%,致命毒性作用通常发生在治疗早期[2]。同年,另一些研究者将目光投向免疫检查点抑制剂相关内分泌功能障碍的问题,此Meta分析报告指出接受PD-1加CTLA-4抑制剂联合治疗的患者发生甲状腺功能障碍和垂体炎的风险增加[3]。
2021年的一项Meta分析评估的是免疫检查点抑制剂相关心脏毒性,研究者指出尽管心脏免疫相关不良事件(irAEs)发病率低,但死亡率高,值得重视[4]。同年另一项Meta分析也关注了心血管(CV)相关irAEs,结果发现ICI的使用与6种CV-irAE的风险增加有关,包括心肌炎,心包疾病,心力衰竭,血脂异常,心肌梗死和脑动脉缺血[5]。
也有研究者关注了免疫治疗中副作用与疗效与获益之间的关系,此项2021年的Meta分析显示,在接受ICI治疗的患者中,irAEs与客观缓解率(ORR)、无进展生存(PFS)期和总生存期(OS)的发展之间存在正相关关系,无论疾病部位、ICIs类型和irAEs。3级或更高的毒性导致更理想的ORR,但更差的OS[6]。
参考文献:
[1]Pala,L.AssociationofAnticancerImmuneCheckpointInhibitorsWithPatient-ReportedOutcomesAssessedinRandomizedClinicalTrials:ASystematicReviewandMeta-analysis.JAMAnetworkopen,5(8),e2226252.https://doi.org/10.1001/jamanetworkopen.2022.26252
[2]Wang,D.Y.FatalToxicEffectsAssociatedWithImmuneCheckpointInhibitors:ASystematicReviewandMeta-analysis.JAMAoncology,4(12),1721–1728.https://doi.org/10.1001/jamaoncol.2018.3923
[3]Barroso-Sousa.IncidenceofEndocrineDysfunctionFollowingtheUseofDifferentImmuneCheckpointInhibitorRegimens:ASystematicReviewandMeta-analysis.JAMAoncology,4(2),173–182.https://doi.org/10.1001/jamaoncol.2017.3064
[4]Rubio-Infant.Cardiotoxicityassociatedwithimmunecheckpointinhibitortherapy:ameta-analysis.Europeanjournalofheartfailure,23(10),1739–1747.https://doi.org/10.1002/ejhf.2289
[5]Dolladille,C.Cardiovascularimmunotoxicitiesassociatedwithimmunecheckpointinhibitors:asafetymeta-analysis.Europeanheartjournal,42(48),4964–4977.https://doi.org/10.1093/eurheartj/ehab618
[6]Hussaini,S.Associationbetweenimmune-relatedsideeffectsandefficacyandbenefitofimmunecheckpointinhibitors-Asystematicreviewandmeta-analysis.Cancertreatmentreviews,92,102134.https://doi.org/10.1016/j.ctrv.2020.102134
MCC码TML0011285-35444,素材失效日2024.10.26
